Modèles de pharmacologie in vivo en Dermatologie
Depuis plus de 20 ans, l’équipe SKINAXIS propose des modèles précliniques en dermatologie reproduisant les modifications physiopathologiques du tissu cutané observées en clinique humaine. SKINAXIS a également développé une expertise unique pour l’évaluation d’innovations en médecine régénérative (greffe de peau, greffe d’organoïdes, substituts cellulaires et acellulaire…) et de dispositifs médicaux pour la cicatrisation.
La valeur translationnelle des modèles SKINAXIS est démontrée par le grand nombre d’innovations thérapeutiques dont les bénéfices ont été confirmés en clinique par la suite.
Les effets de vos molécules et autres innovations thérapeutiques peuvent être évalués grâce à des approches complémentaires et multi-échelles : scoring originaux, fonction de la barrière cutanée, analyses de biomarqueurs. De plus, notre expertise dans le domaine de l’évaluation comportementale ajoute une plus-value translationnelle pour caractériser les effets des composés évalués dans les pathologies inflammatoires telles que le psoriasis, la dermatite atopique et l’eczéma qui induisent des démangeaisons (prurit) et modifient le comportement locomoteur des animaux.
Inflammations cutanées
Les maladies inflammatoires cutanées regroupent un ensemble d’affections caractérisées par une activation anormale du système immunitaire entraînant rougeurs, démangeaisons et altérations de la barrière cutanée.
Notre plateforme vous permet d’évaluer le potentiel de vos candidats sur des modèles prédictifs et avec des outils performants afin de prioriser vos leads au plus fort potentiel translationnel pour prévenir ou traiter ces maladies inflammatoires
Psoriasis – Modèle Imiquimod
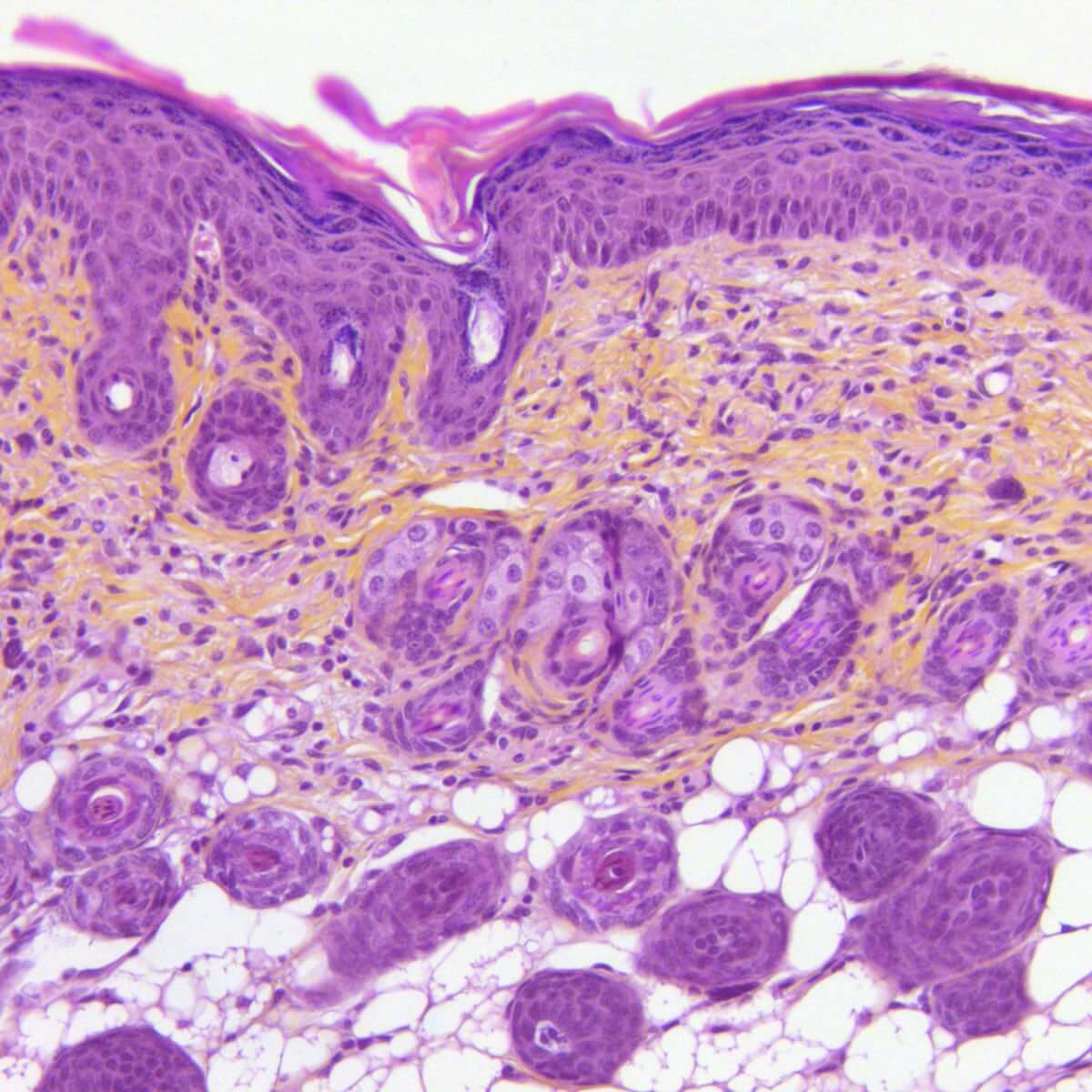
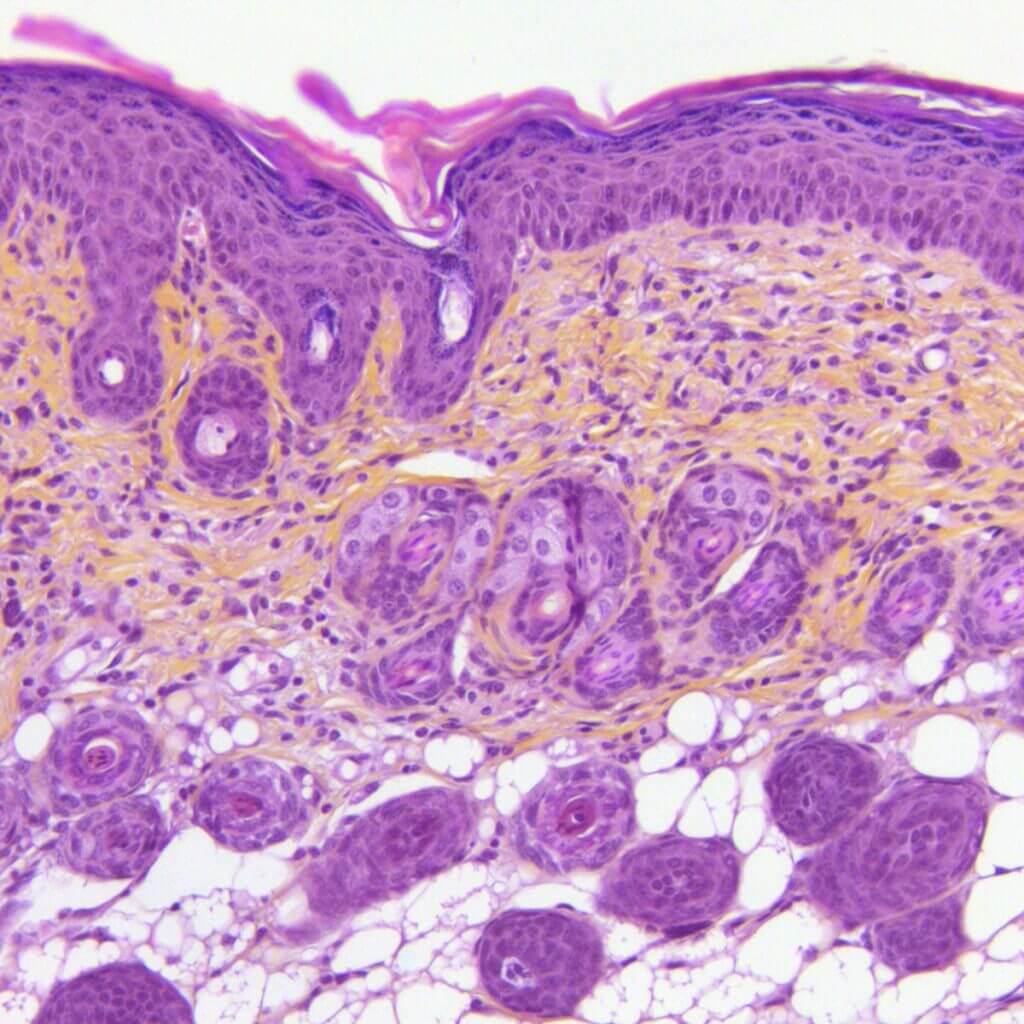
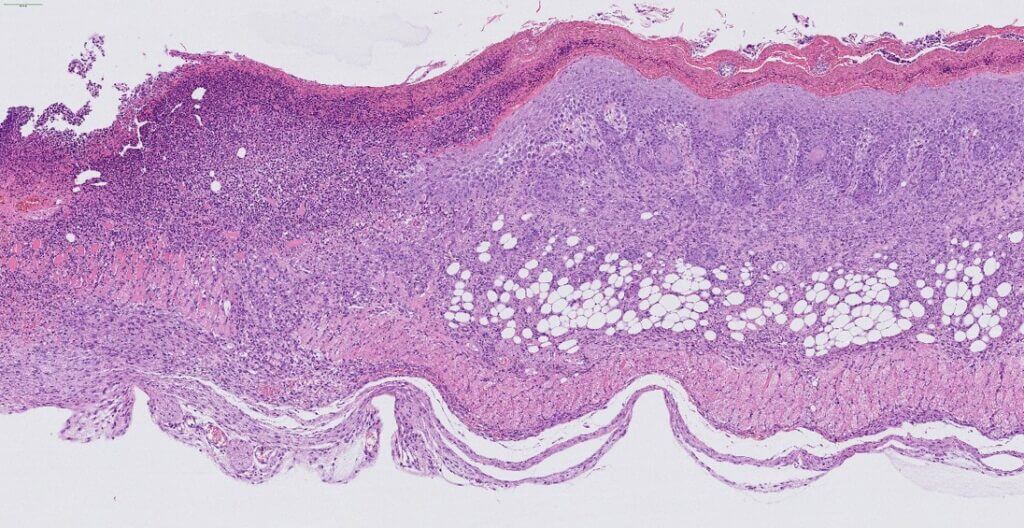
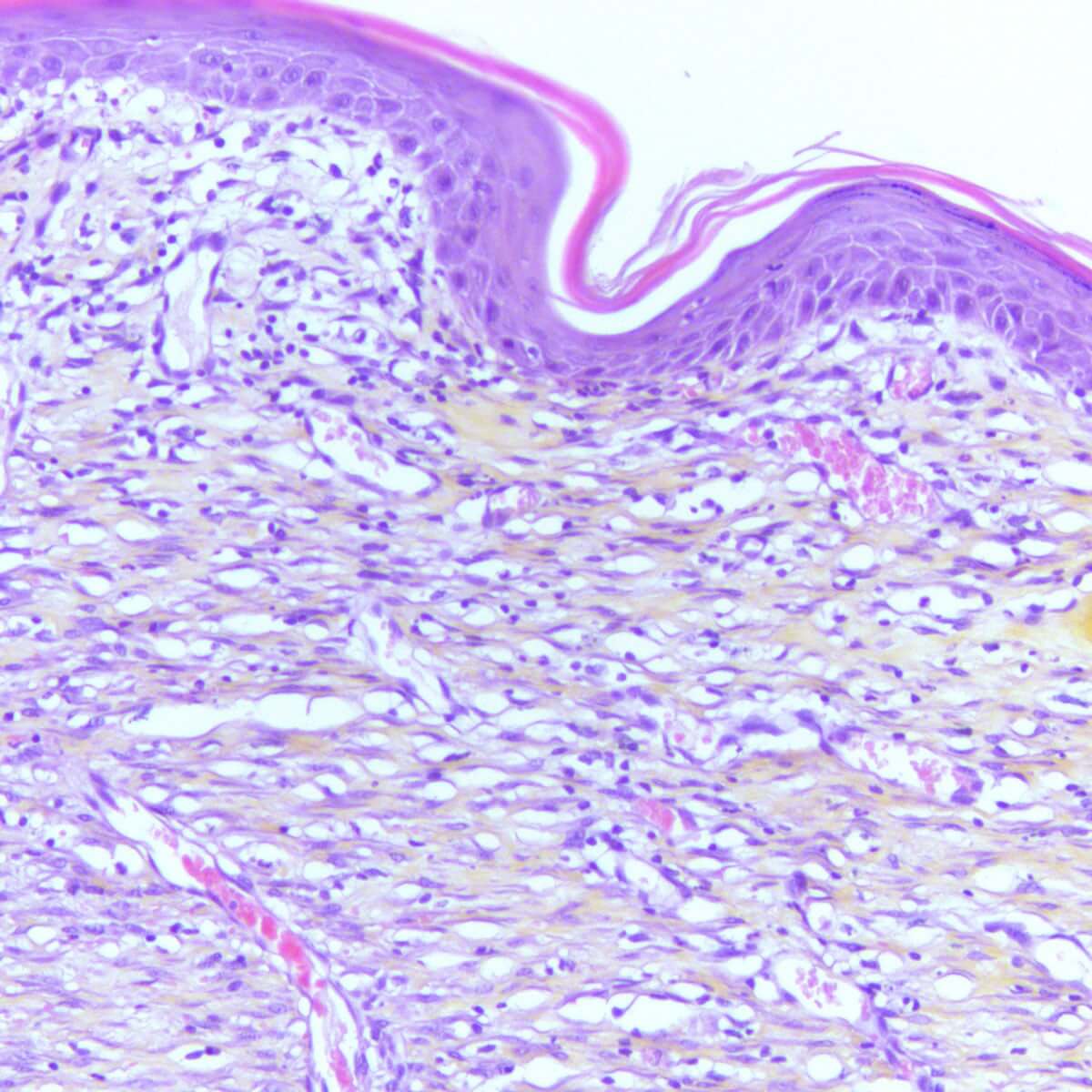
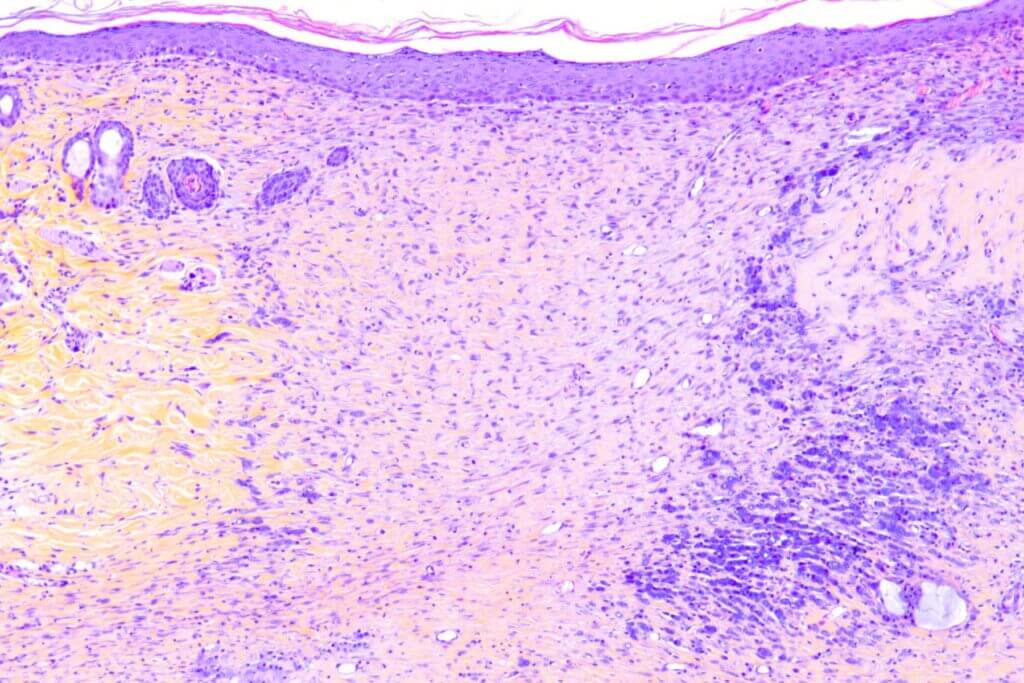
Des applications cutanées répétées d’Imiquimod chez la souris conduisent à la formation progressive d’une inflammation (érythème), d’un oedème et de squames en plaques, modélisant ainsi le psoriasis. Ce modèle, intégrant des mesures in situ (TEWL, dermoscopie, scoring…), une composante comportementale, des dosages de biomarqueurs sériques (IL-17, IL-23, IL-6…) et des analyses histologiques et immunohistochimiques. Il offre une valeur prédictive élevée pour le succès clinique et constitue un outil robuste pour évaluer l’efficacité de vos candidats dans des conditions proches de la physiopathologie humaine.
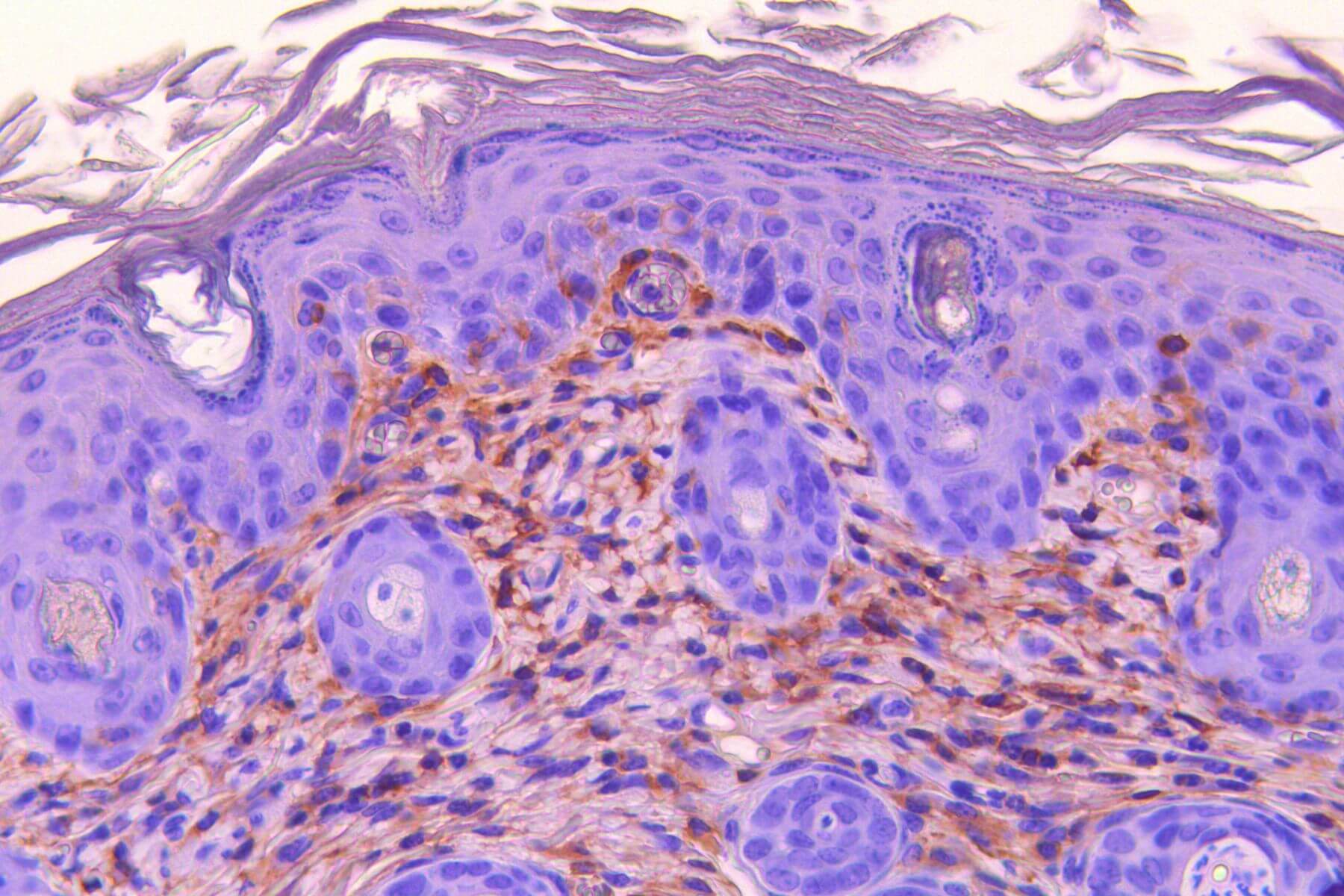
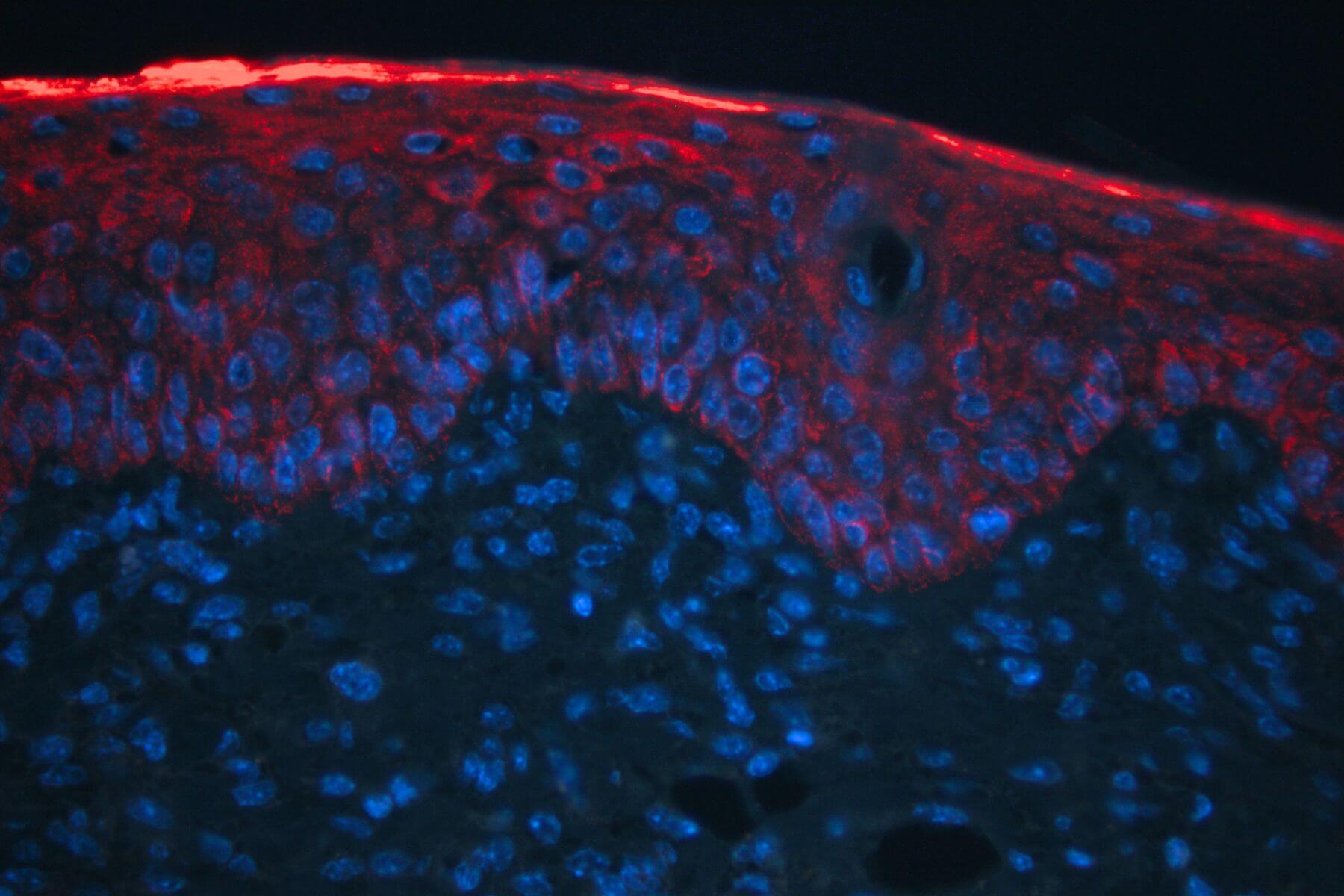
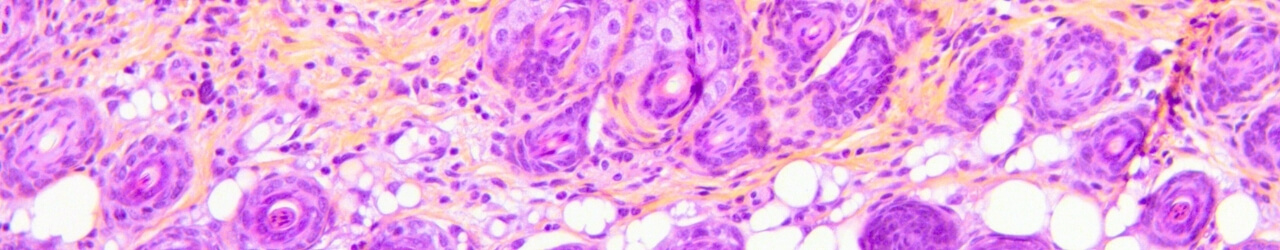
Dermatite atopique - Modèle DNCB
Des applications cutanées répétées de DNCB chez la souris conduisent à la formation progressive d’une inflammation (érythème), d’un oedème, d’érosion et de desquamation de la peau, modélisant ainsi la dermatite atopique. Ce modèle, intégrant des mesures in situ, une composante comportementale, des dosages de biomarqueurs sériques (IL-33, IgE, histamine…) et des analyses histologiques et immunohistochimiques. Il offre une valeur prédictive élevée pour le succès clinique et constitue un outil robuste pour évaluer l’efficacité de vos candidats dans des conditions proches de la physiopathologie humaine.
Eczéma atopique (prurit) – Modèle MC903
Des applications cutanées répétées de MC903 chez la souris conduisent à la production de démangeaisons (prurit) associées à la formation progressive d’une inflammation (érythème), d’un œdème, et de desquamation de la peau, modélisant ainsi l’eczéma atopique. Ce modèle – intégrant des mesures in situ (TEWL, dermoscopie, scoring…), une composante comportementale et des dosages de biomarqueurs sanguins (cytokines) – offre une valeur prédictive élevée pour le succès clinique et constitue un outil robuste pour évaluer l’efficacité de vos candidats dans des conditions proches de la physiopathologie humaine.
Inflammation cutanée chronique
Des applications cutanées répétées de TPA chez la souris conduisent à la formation progressive et durable d’une inflammation qui modélise l’inflammation cutanée chronique. Ce modèle – intégrant des mesures in situ (TEWL, dermoscopie, scoring…), une composante comportementale, des dosages de biomarqueurs sériques (IL-1β, IL-6, TNF-α…) et des analyses histologiques et immunohistochimiques – offre une valeur prédictive élevée pour le succès clinique et constitue un outil robuste pour évaluer l’efficacité de vos candidats dans des conditions proches de la physiopathologie humaine.
Hyperkératose
Des applications cutanées répétées de TPA chez la souris conduisent au développement d’une sécheresse cutanée, un épaississement de la couche cornée et la formation de desquamations, modélisant ainsi l’hyperkératose fréquemment observée dans les verrues.
Ce modèle – intégrant des mesures in situ (TEWL, dermoscopie et scoring) et des analyses histologiques et immunohistochimiques – offre une valeur prédictive élevée pour le succès clinique et constitue un outil robuste pour évaluer l’efficacité de vos candidats dans des conditions proches de la physiopathologie humaine.
Kératose actinique
Une exposition semi-chronique de souris à une dose modérée d’UVB conduit à la formation de lésions cancéreuses bénignes se traduisant par l’apparition de petites plaques rugueuses à la surface de la peau, modélisant ainsi la kératose actinique. Ce modèle, intégrant des mesures in situ (TEWL, dermoscopie, scoring…), offre une valeur prédictive élevée pour le succès clinique et constitue un outil robuste pour évaluer l’efficacité de vos candidats dans des conditions proches de la physiopathologie humaine.
Cancer cutané UVB-induit
Une exposition chronique de souris à une dose modérée d’UVB conduit à la formation de lésions cancéreuses malignes se traduisant par l’apparition de tumeurs à la surface de la peau, modélisant ainsi le cancer cutané UVB-induit. Ce modèle, intégrant des mesures in situ (TEWL, dermoscopie, scoring…), offre une valeur prédictive élevée pour le succès clinique et constitue un outil robuste pour évaluer l’efficacité de vos candidats dans des conditions proches de la physiopathologie humaine.
Douleur à l’application sur une plaie cutanée
À la suite d’une lésion cutanée, la douleur cutanée peut résulter de l’activation directe des nocicepteurs ou d’une inflammation qui active les voies nociceptives. Ce modèle évalue la tolérance aiguë à l’application d’une formulation topique dans des conditions physiologiquement pertinentes.
Cicatrisation
La cicatrisation est un processus biologique complexe par lequel la peau se répare après une lésion, impliquant une succession d’évènements cellulaires, moléculaires et tissulaires afin de restaurer l’intégrité de la barrière cutanée.
Notre plateforme vous permet d’évaluer vos candidats sur des modèles prédictifs avec des outils performants pour évaluer le potentiel de vos candidats sur la cicatrisation de plaies cutanées aiguës et chroniques, afin de prioriser vos leads au plus fort potentiel translationnel.
Plaie cutanée incisionnelle
L’induction d’une plaie cutanée incisionnelle chez la souris ou le rat, sain ou diabétique, correspond à une lésion de la peau provoquée par un objet tranchant, et mime la cicatrisation d’une plaie aiguë.
Ce modèle, intégrant des observations et mesures in situ tout au long du processus cicatriciel, offre une valeur prédictive élevée pour le succès clinique et constitue un outil robuste pour évaluer l’efficacité de vos candidats dans des conditions proches de la physiopathologie humaine.
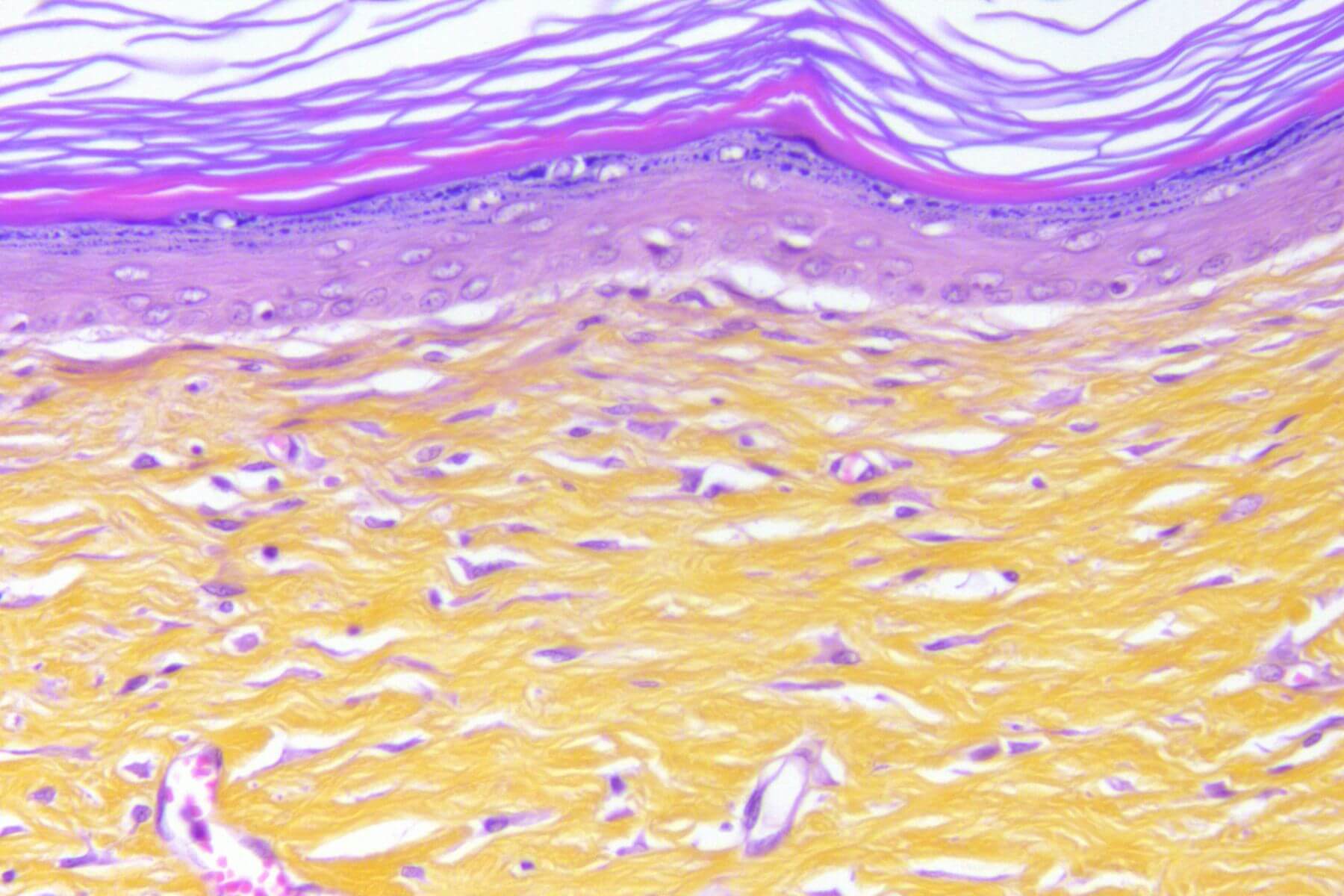
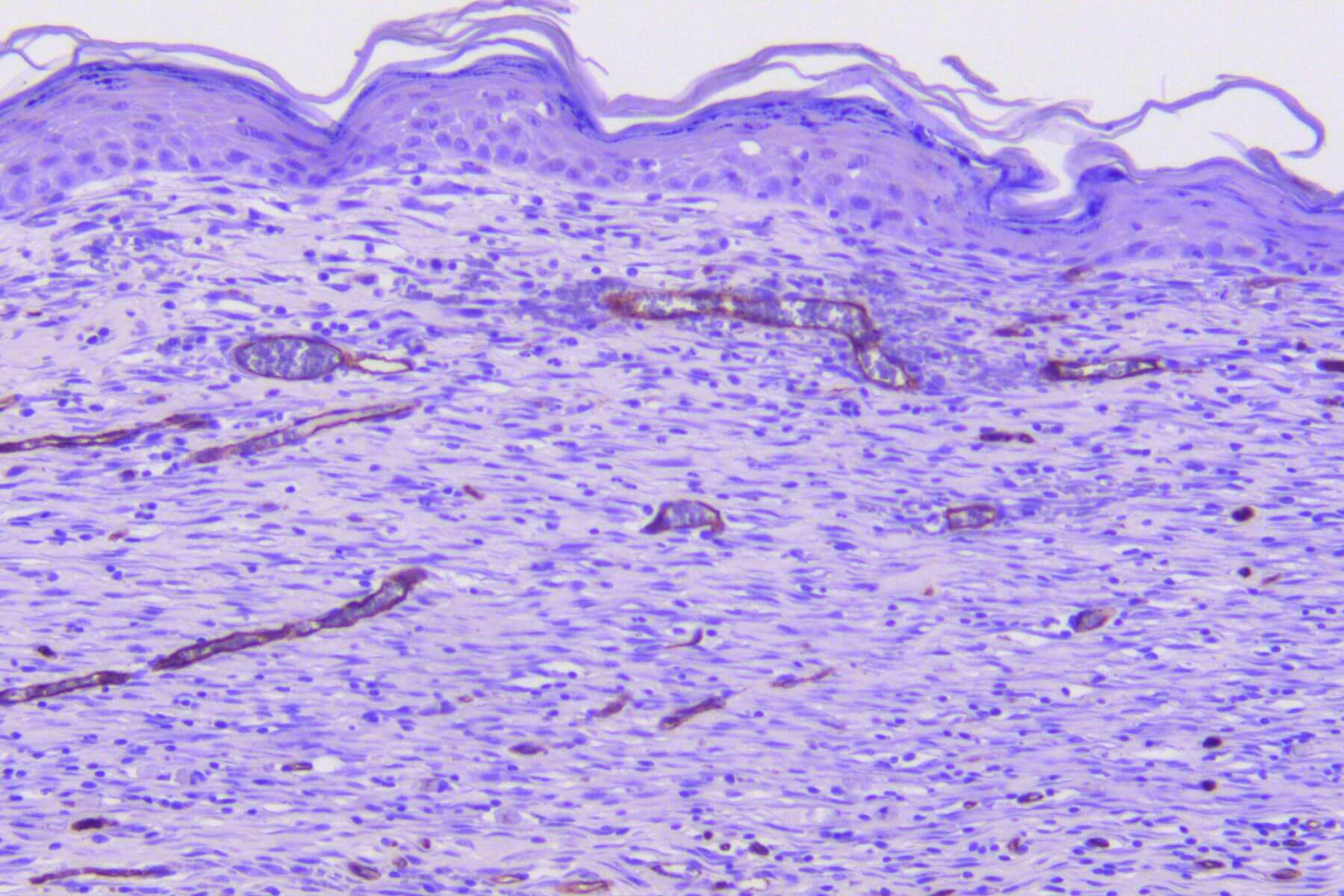
Plaie cutanée excisionnelle
L’induction d’une plaie cutanée exisionnelle chez la souris ou le rat, sain ou diabétique, correspond à une perte de tissu cutané, et mime la cicatrisation d’une plaie aiguë.
Ce modèle, intégrant des observations et mesures in situ (TEWL, dermoscope, scoring…) tout au long du processus cicatriciel, offre une valeur prédictive élevée pour le succès clinique et constitue un outil robuste pour évaluer l’efficacité de vos candidats dans des conditions proches de la physiopathologie humaine.
Ulcération ischémique
L’induction d’une plaie cutanée par ulcération ischémique chez la souris ou le rat, sain ou diabétique, correspond à une perte de tissu cutané importante, et mime la cicatrisation d’une plaie chronique.
Ce modèle, intégrant des observations et mesuresin situ (TEWL, dermoscope, scoring…) tout au long du processus cicatriciel, offre une valeur prédictive élevée pour le succès clinique et constitue un outil robuste pour évaluer l’efficacité de vos candidats dans des conditions proches de la physiopathologie humaine.
Plaie superficielle (abrasion)
L’induction d’une plaie cutanée par abrasion de la peau chez la souris ou le rat, correspond à une lésion traumatique de la peau, et mime la cicatrisation d’une plaie superficielle.
Ce modèle, intégrant des observations et mesures in situ (photos, dermoscope, scoring…) tout au long du processus cicatriciel, offre une valeur prédictive élevée pour le succès clinique et constitue un outil robuste pour évaluer l’efficacité de vos candidats dans des conditions proches de la physiopathologie humaine.
Ampoule
L’induction d’une ampoule par la chaleur et la pression chez la souris, correspond à une lésion superficielle de la peau, et mime la cicatrisation d’une plaie superficielle.
Ce modèle, intégrant des observations et mesures in situ (TEWL, dermoscope, scoring…) tout au long du processus cicatriciel, offre une valeur prédictive élevée pour le succès clinique et constitue un outil robuste pour évaluer l’efficacité de vos candidats dans des conditions proches de la physiopathologie humaine.
Greffes cutanées
Notre savoir-faire unique dans le domaine de la greffe cutanée expérimentale nous permet de tester sur mesure les performances et de la viabilité de vos substituts cutanés. Nous accompagnons nos clients et partenaires dans le domaine de la médecine régénérative afin de traiter les plaies ulcérées, les brûlures graves et les maladies génétiques de la peau. Nous proposons des modèles originaux de plaies excisionnelles complètes, avec une variété de formes, de tailles, et de dispositifs expérimentaux, permettant l’utilisation de substituts cutanés.
Greffe cutanée circulaire
L’induction d’une plaie cutanée circulaire chez la souris ou le rat, immunocompétent ou immunodéficient, correspond à une perte de tissu cutané plus ou moins importante, et mime la cicatrisation d’une plaie cutanée chronique.
Ce modèle, intégrant des observations et mesures in situ (TEWL, dermoscopie, scoring…) tout au long du processus cicatriciel, offre une valeur prédictive élevée pour le succès clinique et constitue un outil robuste pour évaluer l’efficacité de vos candidats dans des conditions proches de la physiopathologie humaine.
Greffe cutanée carrée
L’induction d’une plaie cutanée carrée chez la souris ou le rat, immunocompétent ou immunodéficient, correspond à une perte de tissu cutané importante, et mime la cicatrisation d’une plaie cutanée chronique.
Ce modèle, intégrant des observations et mesures in situ (TEWL, dermoscopie, scoring…) tout au long du processus cicatriciel, offre une valeur prédictive élevée pour le succès clinique et constitue un outil robuste pour évaluer l’efficacité de vos candidats dans des conditions proches de la physiopathologie humaine.
Greffe en Flap
La réalisation d’une greffe en flap chez la souris ou le rat, immunocompétent ou immunodéficient, permet d’évaluer dans des conditions physiologiques anaérobies, l’activité biologique de substituts cutanés.
Ce modèle offre une valeur prédictive élevée pour le succès clinique et constitue un outil robuste pour évaluer l’efficacité de vos candidats dans des conditions proches de la physiopathologie humaine.
Greffe avec insert (cheminée)
La réalisation d’une greffe avec utilisation d’un insert chez la souris ou le rat, immunocompétent ou immunodéficient, permet d’évaluer dans des conditions physiologiques aérobies, l’activité biologique de substituts cutanés.
Ce modèle, intégrant des observations et mesures in situ (TEWL, dermoscopie, scoring…) tout au long du processus cicatriciel, offre une valeur prédictive élevée pour le succès clinique et constitue un outil robuste pour évaluer l’efficacité de vos candidats dans des conditions proches de la physiopathologie humaine.
Toxicité dermique (non BPL)
La toxicité dermique correspond à la capacité d’une substance à induire une atteinte cutanée locale, superficielle, et/ou une toxicité systémique, après pénétration transcutanée et diffusion dans l’organisme.
Notre plateforme vous permet d’évaluer la toxicité dermique de vos candidats de façon aiguë, subchronique et chronique, afin de prioriser vos leads au plus fort potentiel translationnel.
Toxicité dermique aiguë (OCDE 402)
La toxicité dermique aiguë évalue la capacité d’une substance à provoquer des effets indésirables locaux et/ou systémiques après un contact cutané unique.
L’étude est réalisée conformément à la ligne directrice 402 de l’OCDE, dans un cadre de qualité certifié ISO 9001. Elle est idéale pour une réduction précoce des risques liés à vos candidats médicaments avant les études de sécurité BPL.
Toxicité dermique subchronique (OCDE 410)
La toxicité dermique subchronique correspond aux effets indésirables locaux et/ou systémiques survenant après une exposition cutanée répétée à une substance (4 semaines). L’étude est réalisée conformément à la ligne directrice 410 de l’OCDE, dans un cadre de qualité certifié ISO 9001. Elle est idéale pour une réduction précoce des risques liés à vos candidats médicaments avant les études de sécurité BPL.
Toxicité dermique chronique (OCDE 411)
La toxicité dermique chronique correspond aux effets indésirables locaux et/ou systémiques survenant après une exposition cutanée prolongée et répétée à une substance sur une longue durée (13 semaines). L’étude est réalisée conformément à la ligne directrice 411 de l’OCDE, dans un cadre de qualité certifié ISO 9001. Elle est idéale pour une réduction précoce des risques liés à vos candidats médicaments avant les études de sécurité BPL.
Pharmacocinétique (PK) et neuro-PK
Nos études de pharmacocinétique s’appuient sur des cinétiques flexibles adaptées à votre candidat médicament. Nous analysons les matrices biologiques classiques (plasma, sérum, LCR) ainsi que des organes ou régions anatomiques clés, afin de caractériser précisément l’exposition tissulaire de votre molécule.
Ces approches robustes et personnalisables sécurisent vos décisions précliniques.
Modèle pharmacocinétique (PK)
Nous proposons des études adaptées à vos besoins en PK et Neuro-PK, couvrant différentes voies d’administration (sous-cutanée, intrapéritonéale, intraveineuse, orale, intranasale, etc.), en traitement aiguë ou chronique. Nous mesurons la biodisponibilité de vos molécules dans différents compartiments : sang, cerveau (BBB), liquide céphalo-rachidien ou tout autre tissu d’intérêt. Cette approche vous garantit des données fiables pour orienter vos décisions et accélérer le développement de vos traitements.
Disponible chez la souris, le rat et le porc.
Autres maladies inflammatoires
Les maladies inflammatoires se caractérisent par le recrutement et l’activation de cellules inflammatoires et la formation de lésions d’aspect très divers pouvant atteindre l’ensemble des organes du corps humain.
Notre plateforme vous permet d’évaluer directement vos candidats sur des organes cibles grâce à des modèles prédictifs et des outils analytiques performants pour sélectionner et évaluer vos candidats les plus prometteurs et optimiser la dose et le schéma thérapeutique afin de maximiser les résultats thérapeutiques. Cela permet de prioriser vos leads au plus fort potentiel translationnel.
Ulcération colique (TNBS)
Une administration intrarectale unique de TNBS chez le rat conduit à la formation d’une ulcération de la paroi colique résultant de l’agression inflammatoire générée par le TNBS.
Ce modèle, intégrant des mesures in situ exclusives (coloscopie) et une composante comportementale, offre une valeur prédictive élevée pour le succès clinique et constitue un outil robuste pour évaluer l’efficacité de vos candidats dans des conditions proches de la physiopathologie humaine.
Cystite (Cyclophosphamide)
Une ou plusieurs administrations par voie générale de cyclophosphamide chez le rat conduit à la formation d’une inflammation aiguë ou chronique de la vessie, résultant de la métabolisation de la cyclophosphamide.
Ce modèle, qui intègre une composante comportementale, offre une valeur prédictive élevée pour le succès clinique et constitue un outil robuste pour évaluer l’efficacité de vos candidats dans des conditions proches de la physiopathologie humaine.
Fibrose hépatique (Phénobarbital/CCl4)
Des administrations répétées à dose croissante de tétrachlorure de carbone (CCl4,) chez le rat préalablement exposés au phénobarbital, conduit à la formation d’une toxicité hépatique générant une inflammation progressant vers une fibrose hépatique.
Ce modèle, intégrant une composante comportementale, offre une valeur prédictive élevée pour le succès clinique et constitue un outil robuste pour évaluer l’efficacité de vos candidats dans des conditions proches de la physiopathologie humaine.
Hyperplasie bénigne de la prostate (Testostérone)
Des administrations répétées de testostérone chez le rat mâle conduit à la formation d’une d’inflammation progressant vers la formation d’une augmentation bénigne du volume de la prostate dite hyperplasie bénigne de la prostate.
Ce modèle offre une valeur prédictive élevée pour le succès clinique et constitue un outil robuste pour évaluer l’efficacité de vos candidats dans des conditions proches de la physiopathologie humaine.
Diarrhée (Huile de Ricin)
Une administration intragastrique unique d’huile de ricin chez le rat conduit à la formation d’une inflammation aiguë de la muqueuse intestinale et la production d’une diarrhée.
Ce modèle, intégrant une composante comportementale avec un scoring exclusif, offre une valeur prédictive élevée pour le succès clinique et constitue un outil robuste pour évaluer l’efficacité de vos candidats dans des conditions proches de la physiopathologie humaine.
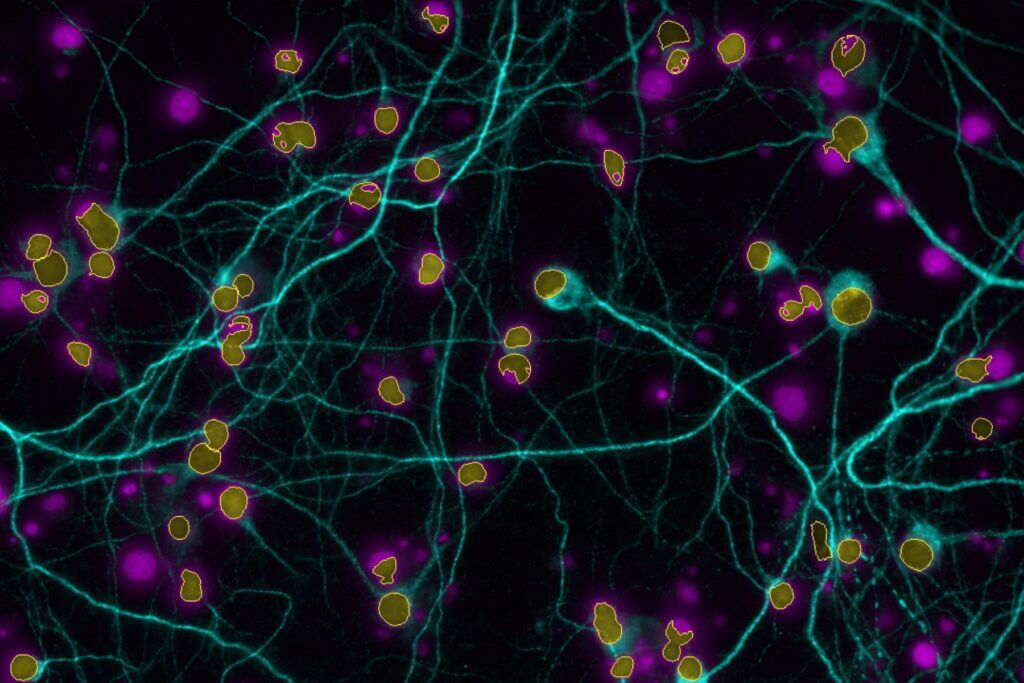
High-Content Imaging
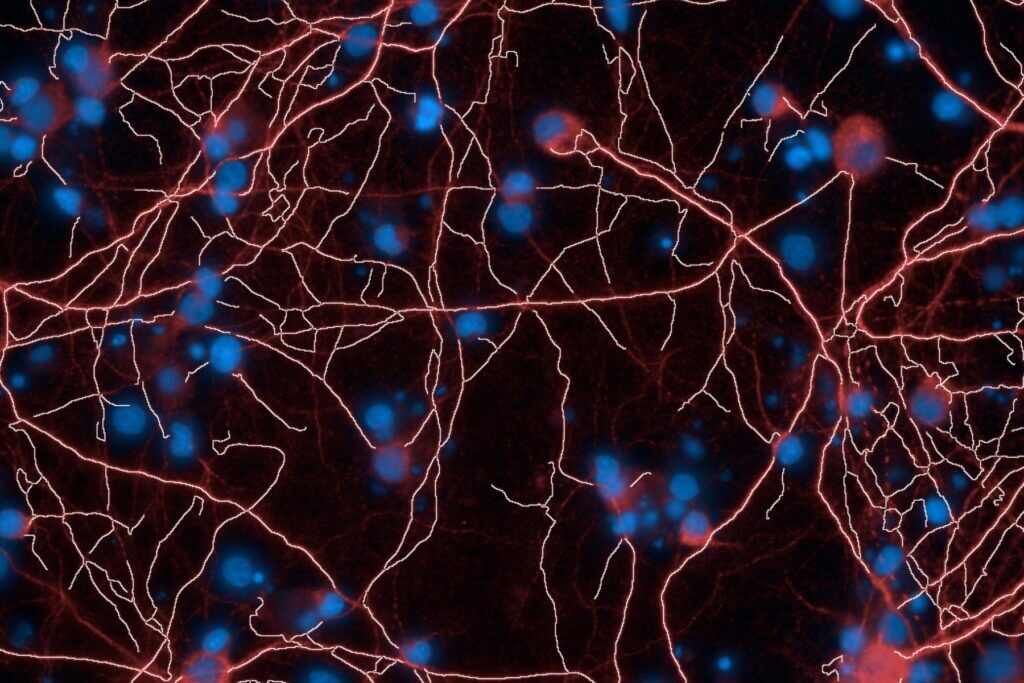
Microfluidique et cerveaux-sur-puce

Animaleries petits et gros animaux
Imagerie médicale préclinique

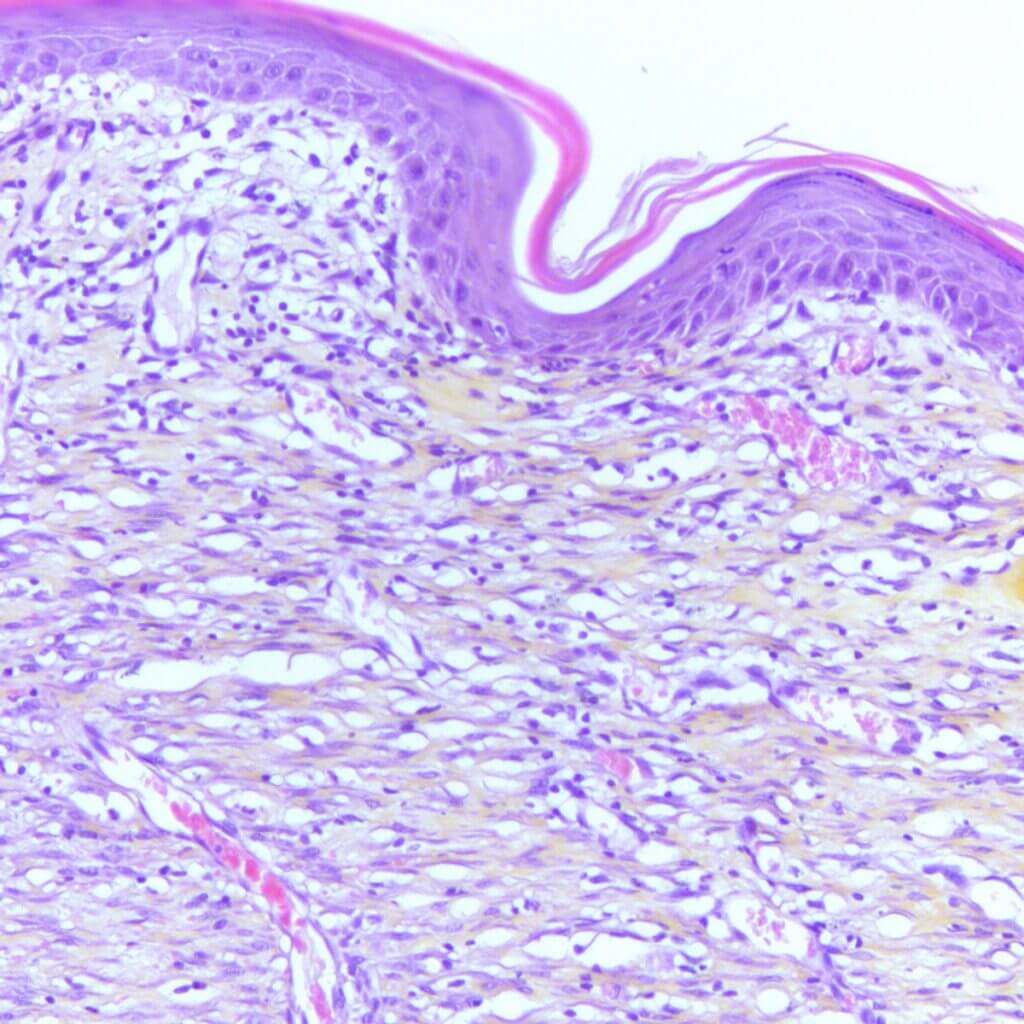
Immunohistochimie, immunofluorescence et histologie
Immunodosage
Les effets de vos molécules peuvent être évalués grâce à des approches complémentaires et multi-échelles.