Modèles de pharmacologie in vivo en Cardiovasculaire
Depuis plus de 25 ans, SYNCROSOME possède une expertise pointue dans les principales maladies cardiovasculaires (hypertension artérielle pulmonaire, ischémie-reperfusion, insuffisance cardiaque…) et cardiométaboliques pour la réalisation d’études pharmacologiques in vivo. Nous disposons des connaissances, des compétences et de la plateforme in vivo nécessaires pour tester l’efficacité de vos agents thérapeutiques. Pour les techniques invasives cardiovasculaires, nous possédons des blocs opératoires agréés et une équipe technique qualifiée. Nos modèles rongeurs (rats ou souris selon la pathologie) sont adaptés aux tests de médicaments modificateurs de la maladie ou de composés agissant sur les symptômes.
Insuffisance cardiaque droite
L’insuffisance cardiaque droite se caractérise par l’incapacité du ventricule droit à assurer efficacement l’éjection du sang vers les poumons. Cette défaillance résulte souvent d’une augmentation chronique de la pression dans l’artère pulmonaire, comme c’est le cas dans l’hypertension artérielle pulmonaire. Face à cette surcharge persistante, le ventricule droit se remodèle, s’épuise progressivement ce qui finit par mener à une insuffisance cardiaque droite.
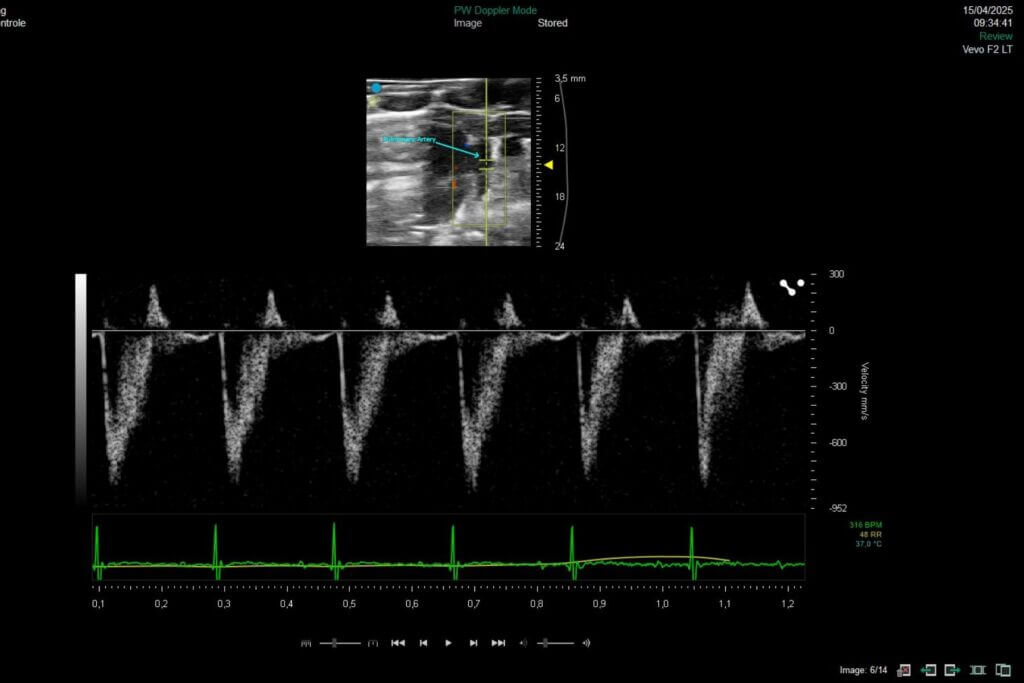
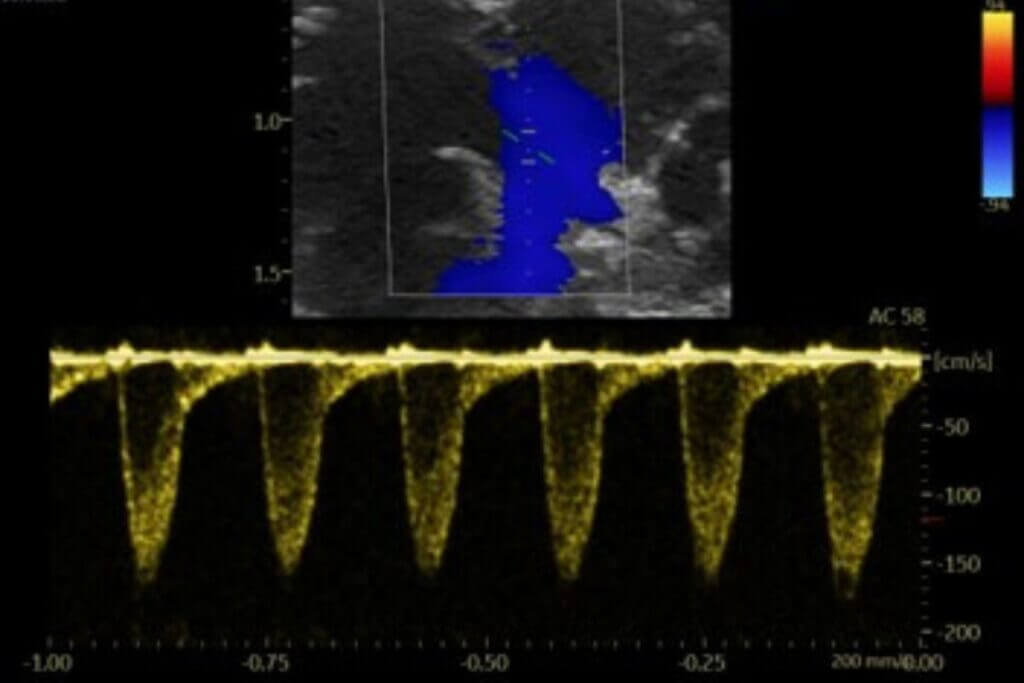
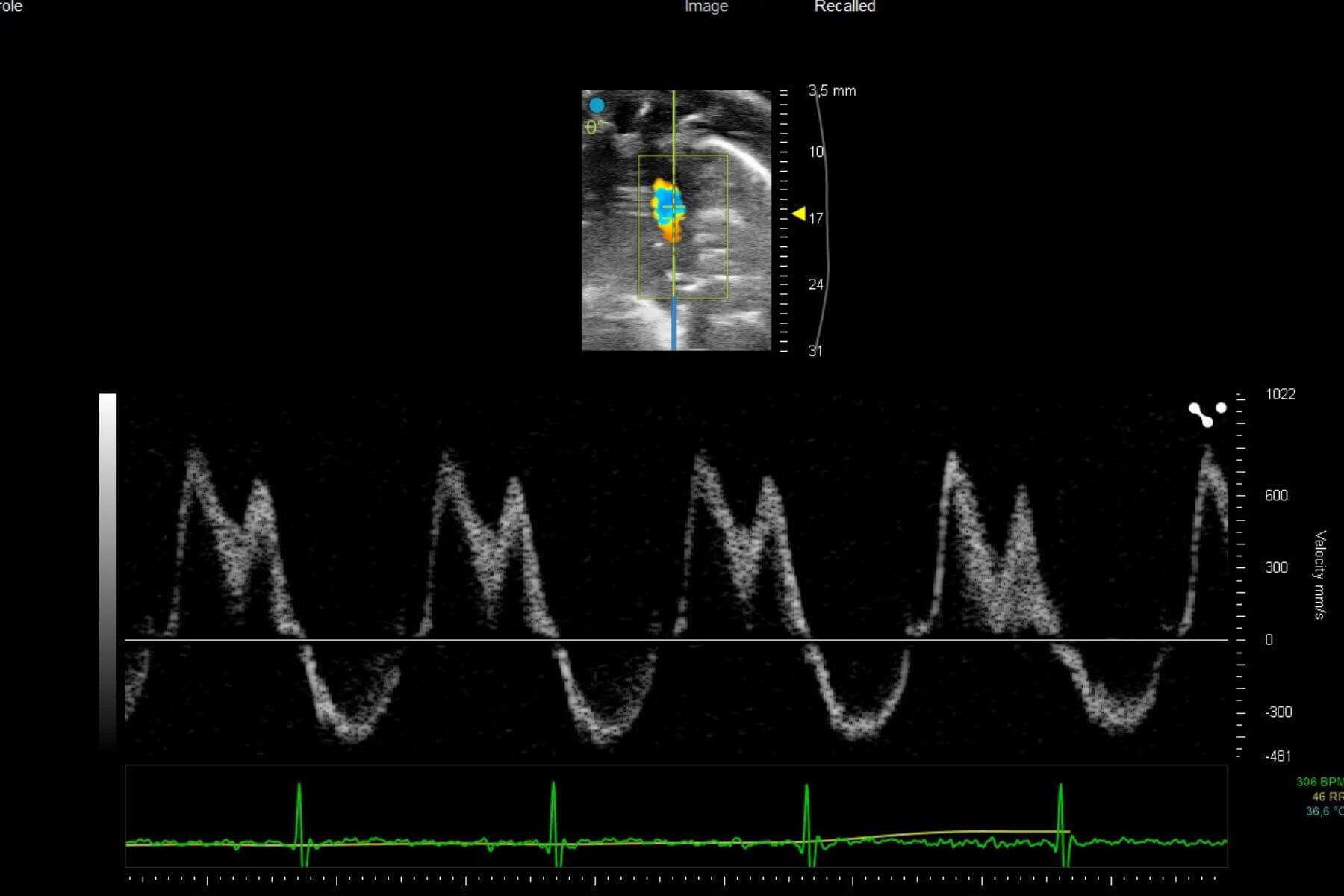
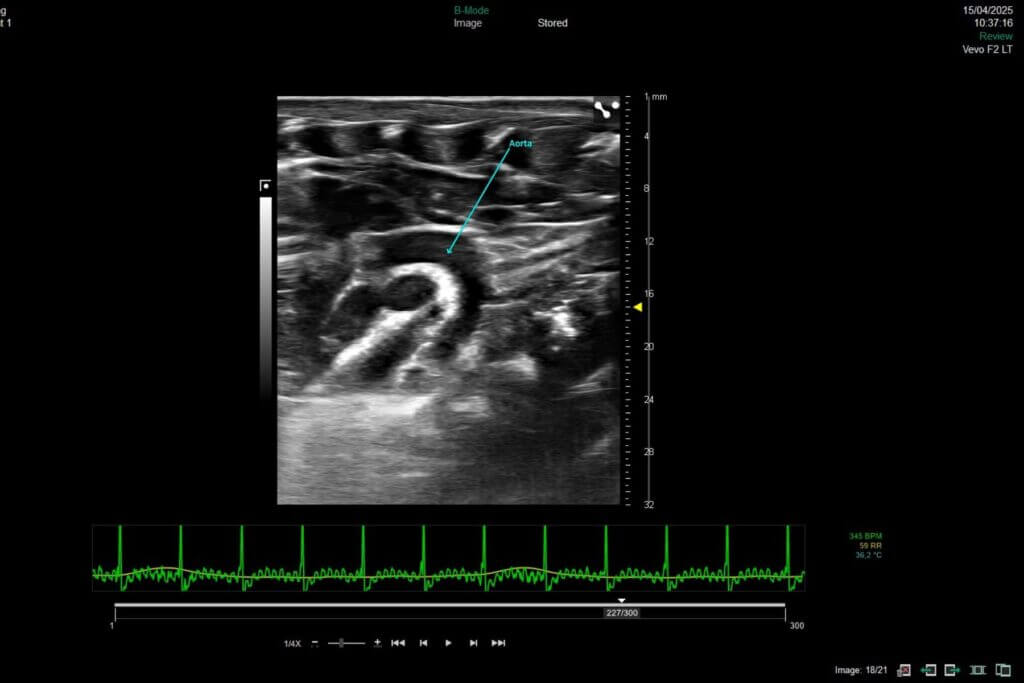
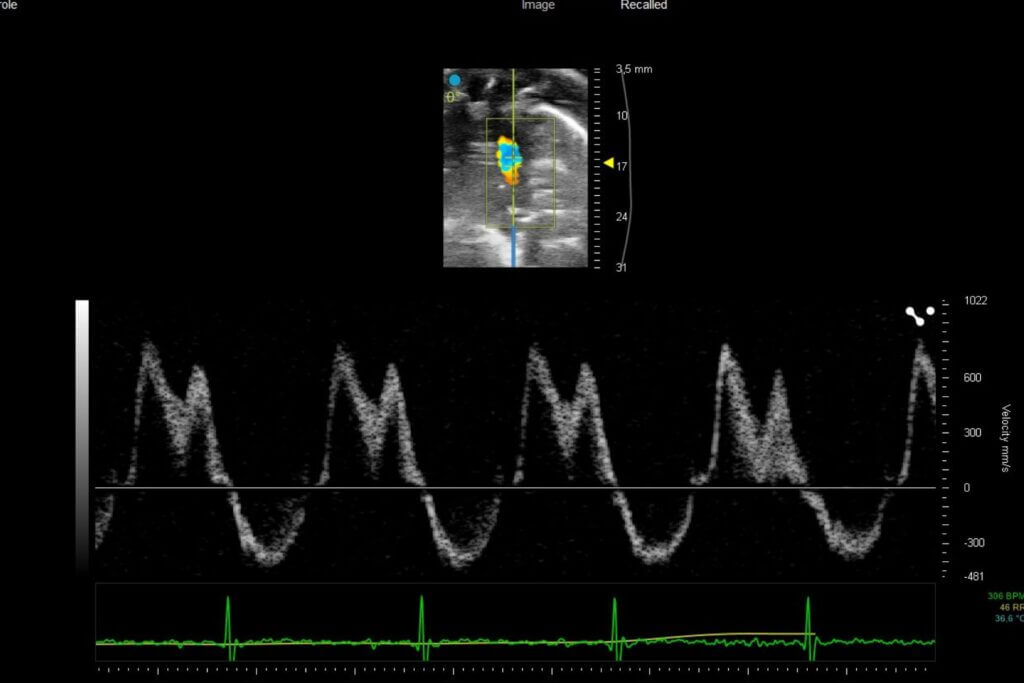
Notre plateforme vous permet d’évaluer directement l’effet de vos candidats dans des modèles pathologiques clés et d’étudier l’impact sur la fonction cardiaque et le remodelage pulmonaire et vasculaire.
Hypertension artérielle pulmonaire (PAH)
Hypoxie chronique
Le modèle d’hypoxie est un classique pour induire une hypertension artérielle pulmonaire modérée chez l’animal. Il repose sur l’induction d’une hypoxie chronique à l’aide de caissons d’hypoxie spécialement conçus à cet effet. Le modèle se caractérise par une vasoconstriction pulmonaire persistante, suivie d’un remodelage modéré des artères pulmonaires.
Modèle établi chez le rat.
Sugen-Hypoxie
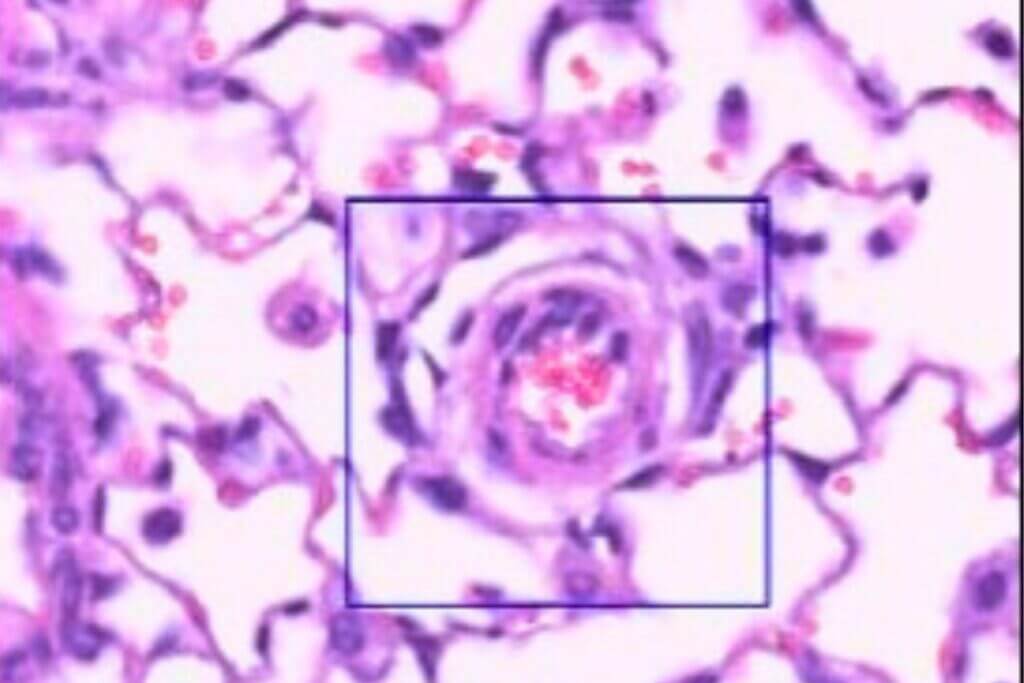
Le modèle SUGEN-hypoxie combine l’injection d’un inhibiteur du récepteur au VEGF à une exposition prolongée à l’hypoxie pour induire une hypertension pulmonaire progressive et sévère accompagnée d’une insuffisance cardiaque du ventricule droit. Ce modèle récapitule la majorité des manifestations cliniques observées chez l’humain, y compris les lésions plexiformes des artérioles pulmonaires. Il constitue le modèle de référence pour étudier les formes avancées de PAH ce qui permet d’évaluer l’efficacité de thérapies ciblant le remodelage vasculaire complexe, la prolifération cellulaire ou la dysfonction endothéliale. Sa sévérité et sa stabilité en font un outil puissant pour générer des données précliniques à fortes valeurs translationnelles.
Modèle établi chez le rat.
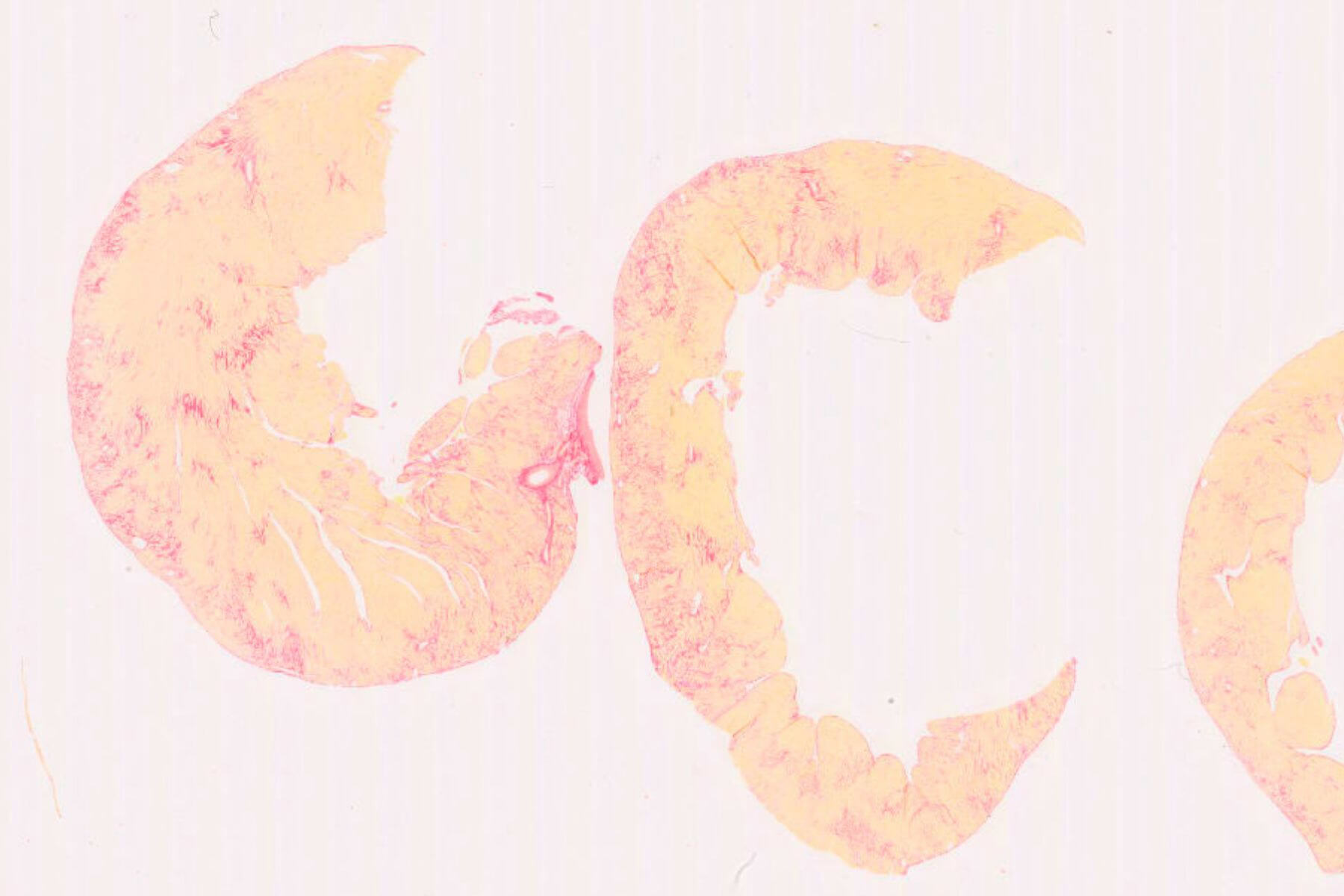
Monocrotaline (MCT)
Le modèle monocrotaline (MCT) est l’un des plus utilisés pour l’induction expérimentale de PAH. Une injection unique de MCT entraîne une atteinte endothéliale et inflammatoire marquée des artérioles pulmonaires, similaire à celle observée en clinique humaine, suvie d’un remodelage vasculaire progressif et d’une hypertrophie du ventricule droit. Ce modèle cours est utile pour le screening rapide de thérapies ciblant diverses caractéristiques propres à la PAH. Sa cinétique bien connue permet d’optimiser les fenêtres thérapeutiques et de générer des données robustes pour démontrer l’efficacité de votre candidats médicaments.
Modèle établi chez le rat.
Embolie pulmonaire
L’embolie pulmonaire correspond à l’obstruction brutale d’une ou plusieurs artères pulmonaires par un embole, le plus souvent un caillot sanguin. Cette obstruction entraîne une diminution du flux sanguin vers une partie du poumon, provoquant une altération des échanges gazeux et une surcharge aiguë du ventricule droit.
Modèle d’embolie pulmonaire par injection de caillots autologues
Le modèle d’embolie pulmonaire par injection de caillots autologues consiste à préparer l’injection de caillots préfabriqué et calibrés dans la veine jugulaire afin d’obstruer sélectivement les artères pulmonaires. Ce modèle reproduit l’augmentation aiguë de la pression pulmonaire observée en clinique humaine, avec un stress important sur le ventricule droit et un remodelage vasculaire secondaire. La sévérité de l’atteinte peut être adaptée en fonction de la quantité de matériel thrombotique utilisée. La bonne reproductibilité et la rapidité de mise en œuvre permettent d’évaluer rapidement l’efficacité de traitements thrombolytiques, vasodilatateurs ou cardioprotecteurs.
Modèle établi chez le rat.
Insuffisance cardiaque gauche
L’insuffisance cardiaque gauche se caractérise par l’incapacité du ventricule gauche à fournir un débit cardiaque adéquat aux besoins de la circulation systémique. Elle résulte de contraintes chroniques telles qu’une augmentation de la postcharge ou des atteintes myocardiques ischémiques et s’accompagne d’un remodelage structurel et fonctionnel.
Notre plateforme vous permet d’évaluer directement l’effet de vos candidats thérapeutiques autant dans des modèles d’HFrEF que d’HFpEF et inclue les analyses de la fonction ventriculaire gauche par échocardiographie, le remodelage cardiaque et les interactions cœur-rein-métabolisme.
Insuffisance cardiaque gauche à fraction d’éjection réduite (HFrEF)
Suite à une cardiopathie ischémique étendue ou un infarctus du myocarde, la pathologie évolue fréquemment vers une réduction de la fraction d’éjection cardiaque qui définit l’HFrEF.
Nos modèles chez le rats reproduisent les principales caractéristiques de l’HFrEF humaine.
Modèle d’ischémie permanente de l’artère coronaire
Le modèle d’ischémie permanente de l’artère coronaire gauche repose sur la ligature définitive de cette artère, provoquant un infarctus du myocarde étendu et une défaillance progressive du ventricule gauche. Il reproduit fidèlement les mécanismes de remodelage post‑infarctus : nécrose, inflammation, fibrose et altération durable de la fonction cardiaque. Ce modèle constitue un outil robuste pour évaluer des thérapies cardioprotectrices, antifibrotiques ou régénératives.
Modèle établi chez le rat.
Modèle d’ischémie-reperfusion (IRI)
Le modèle d’ischémie‑reperfusion myocardique (IRI) consiste à occlure temporairement l’artère coronaire gauche, puis à restaurer le flux sanguin afin de reproduire les lésions induites par la reperfusion après un infarctus traité. Cette approche génère un stress oxydatif massif, une inflammation aiguë, une apoptose importante et un remodelage précoce du myocarde. Ce modèle offre une plateforme idéale pour évaluer des thérapies cardioprotectrices, antioxydantes ou anti‑inflammatoires ciblant les dommages de reperfusion.
Modèle établi chez le rat.
Modèle de lésion cardiaque induite par l’isoprotérénol
Le modèle de lésion cardiaque induite par l’isoprotérénol repose sur l’administration répétée de ce β‑agoniste synthétique, induisant un stress cardiaque aigu qui conduit à une nécrose myocardique, une inflammation marquée et un remodelage rapide du ventricule gauche. Il reproduit des lésions diffuses proches de celles observées lors de myocardites ou de cardiomyopathies induites par le stress. Ce modèle offre une mise en œuvre simple et une cinétique rapide. Il constitue un outil efficace pour évaluer des thérapies cardioprotectrices, anti‑inflammatoires ou antifibrotiques.
Modèle établi chez le rat.
Insuffisance cardiaque gauche à fraction d’éjection préservée (HFpEF)
L’HFpEF se caractérise par une altération du remplissage ventriculaire liée à une rigidité myocardique accrue, malgré une fonction systolique conservée. L’HFpEF est étroitement associée aux maladies métaboliques telles que l’obésité, le diabète de type 2 et le syndrome métabolique, ainsi qu’à l’insuffisance rénale chronique qui contribue à son aggravation.
Nos modèles rongeurs reproduisent les altérations de la fonction cardiaque caractéristiques de l’HFpEF, en lien avec différentes combinaisons de comorbidités métaboliques.
Modèle de rat Dahl
Le modèle des rats Dahl sensibles au sel reproduit de manière progressive et physiologique les mécanismes de la HFpEF. Exposés à un régime riche en sel, ces animaux développent une hypertension sévère, un remodelage concentrique du ventricule gauche, une fibrose myocardique et une altération de la relaxation cardiaque, tout en conservant une fraction d’éjection préservée.
Modèle établi chez le rat.
Souris BTBR ob/ob
Le modèle des souris BTBR ob/ob reproduit une forme métabolique de HFpEF, caractérisée par une obésité sévère, une résistance à l’insuline, une insuffisance rénale et une dysfonction diastolique progressive. Ces animaux développent un remodelage concentrique du ventricule gauche, une fibrose myocardique et une altération de la relaxation cardiaque, tout en conservant une fraction d’éjection préservée.
Modèle établi chez la souris.
Souris db/db
Le modèle des souris db/db reproduit un syndrome métabolique de HFpEF liée à l’obésité sévère et au diabète de type 2. Ces animaux développent une résistance à l’insuline, une inflammation systémique, une fibrose myocardique et une altération progressive de la relaxation ventriculaire, avec une fraction d’éjection qui reste préservée.
Modèle établi chez la souris.
Modèle L-NAME + régime gras
Le modèle combinant L‑NAME et un régime riche en graisses (HFD) reproduit une forme multifactorielle de HFpEF, associant hypertension, dysfonction endothéliale, obésité et inflammation systémique. L’inhibition de la synthèse du NO par le L‑NAME induit une élévation marquée de la pression artérielle, tandis que le HFD favorise le développement d’un syndrome métabolique avec un remodelage concentrique, la fibrose myocardique et la dysfonction diastolique, tout en maintenant une fraction d’éjection préservée.
Modèle établi chez la souris.
Fibrinolyse et anticoagulants
Modèle d’embolie pulmonaire
Modèle d’embolie pulmonaire par injection de caillots autologues
Le modèle d’embolie pulmonaire par injection de caillots autologues consiste à préparer l’injection de caillots préfabriqué et calibrés dans la veine jugulaire afin d’obstruer sélectivement les artères pulmonaires. Ce modèle reproduit l’augmentation aiguë de la pression pulmonaire observée en clinique humaine, avec un stress important sur le ventricule droit et un remodelage vasculaire secondaire. La sévérité de l’atteinte peut être adaptée en fonction de la quantité de matériel thrombotique utilisée. La bonne reproductibilité et la rapidité de mise en œuvre permettent d’évaluer rapidement l’efficacité de traitements thrombolytiques, vasodilatateurs ou cardioprotecteurs.
Modèle établi chez le rat.
AVC Thromboembolique
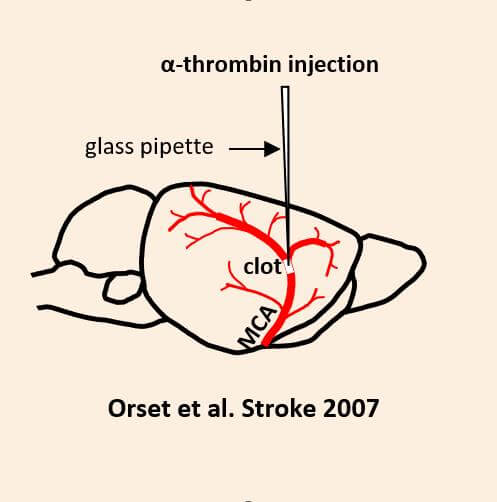
Occlusion de l’ACM par injection de thrombine
Ce modèle préclinique d’AVC ischémique est induit par formation d’un caillot riche en fibrine dans l’AC. Ce caillot est efficacement lysé par les fibrinolytiques standards cliniques (Alteplase, Tenecteplase), modélisant la sous-population de patients qui répond aux traitements de référence, ce qui en fait de ce modèle un outil translationnel de référence pour évaluer l’efficacité de vos candidats thrombolytiques. Ce modèle est également pertinent pour l’évaluation de composés neuroprotecteurs dans une situation expérimentale mimant la réalité clinique de la phase aigüe de l’AVC (présence d’un thrombi et recanalisation pharmacologique dans une fenêtre thérapeutique pertinente). Il permet notamment d’étudier les interactions avec les traitements fibrinolytiques de référence.
Ce modèle est établi chez la souris.
Occlusion de l’ACM par application de FeCl₃ ou AlCl₃
Ce modèle préclinique d’AVC ischémique est induit par la formation d’un caillot riche en plaquettes, résistant aux fibrinolytiques de référence (Alteplase, Tenecteplase), mais sensible à des d’autres agents thrombolytiques tels que la N-acétylcystéine. En modélisant la sous-population de patients non-répondeurs aux traitements standards, ce modèle translationnel constitue un outil clé pour évaluer l’efficacité et la supériorité de vos candidats, les combinaisons de traitements ou les interactions pharmacologiques.
Ce modèle est établi chez la souris.
Occlusion thromboembolique de la ACM – Injection de caillots autologues
L’injection de caillots autologues vers l’ACM induit des lésions corticales et sous‑corticales, reflétant la physiopathologie thrombotique observée en clinique. Sensible au traitement fibrinolytique de référence (Alteplase), ce modèle original permet d’évaluer un large panel de candidats, d’explorer les interactions thérapeutiques et de suivre la récupération sensorimotrice et cognitive jusqu’au long terme.
IHC par injection de collagénaseL’injection stéréotaxique de collagénase déstabilise le mur vasculaire induisant un saignement à l’origine de la formation d’un hématome ainsi qu’une réponse inflammatoire. Ce modèle d’AVC hémorragique constitue un outil translationnel pour évaluer l’efficacité de vos molécules sur les saignements, l’inflammation et la neuroprotection. Suivant vos besoins, il offre également la possibilité d’évaluer le risque de sursaignement.
Ce modèle est établi chez le rat.
AVC hémorragique
IHC par injection de collagénase
L’injection stéréotaxique de collagénase déstabilise le mur vasculaire induisant un saignement à l’origine de la formation d’un hématome ainsi qu’une réponse inflammatoire. Ce modèle d’AVC hémorragique constitue un outil translationnel pour évaluer l’efficacité de vos molécules sur les saignements, l’inflammation et la neuroprotection. Suivant vos besoins, il offre également la possibilité d’évaluer le risque de sursaignement (safety).
Modèle de saignement
Temps de saignement à la queue
Le test de saignement à la queue est un gold-standard utilisé pour évaluer l’hémostase et la fonction plaquettaire in vivo.
Ce modèle est sensible aux traitements anticoagulants et fibrinolytiques couramment administrés en clinique comme l’héparine, les anticoagulants direct oraux ou l’Alteplase. Il permet ainsi d’évaluer l’efficacité de composés candidats de différentes classes telles que les anti-coagulants, les pro-coagulants ou les inhibiteurs plaquettaires.
Ce modèle est établi chez la souris.
Pharmacocinétique (PK) et neuro-PK
Nos études de pharmacocinétique s’appuient sur des cinétiques flexibles adaptées à votre candidat médicament. Nous analysons les matrices biologiques classiques (plasma, sérum, LCR) ainsi que des organes ou régions anatomiques clés, afin de caractériser précisément l’exposition tissulaire de votre molécule.
Ces approches robustes et personnalisables sécurisent vos décisions précliniques.
Modèle pharmacocinétique (PK)
Nous proposons des études adaptées à vos besoins en PK et Neuro-PK, couvrant différentes voies d’administration (sous-cutanée, intrapéritonéale, intraveineuse, orale, intranasale, etc.), en traitement aiguë ou chronique. Nous mesurons la biodisponibilité de vos molécules dans différents compartiments : sang, cerveau (BBB), liquide céphalo-rachidien ou tout autre tissu d’intérêt. Cette approche vous garantit des données fiables pour orienter vos décisions et accélérer le développement de vos traitements.
Disponible chez la souris, le rat et le porc.
High-Content Imaging
Microfluidique et cerveaux-sur-puce

Animaleries petits et gros animaux
Imagerie médicale préclinique

Immunohistochimie, immunofluorescence et histologie
Immunodosage
Les effets de vos molécules peuvent être évalués grâce à des approches complémentaires et multi-échelles.