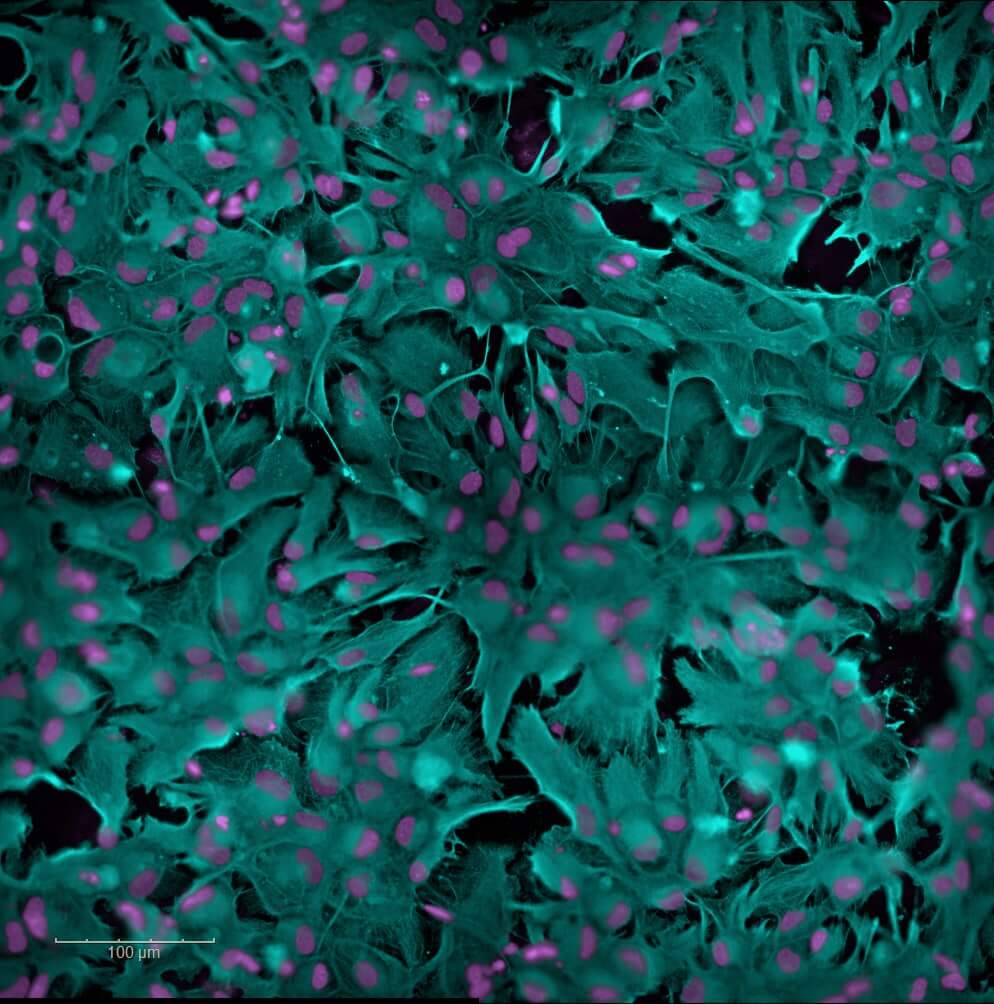
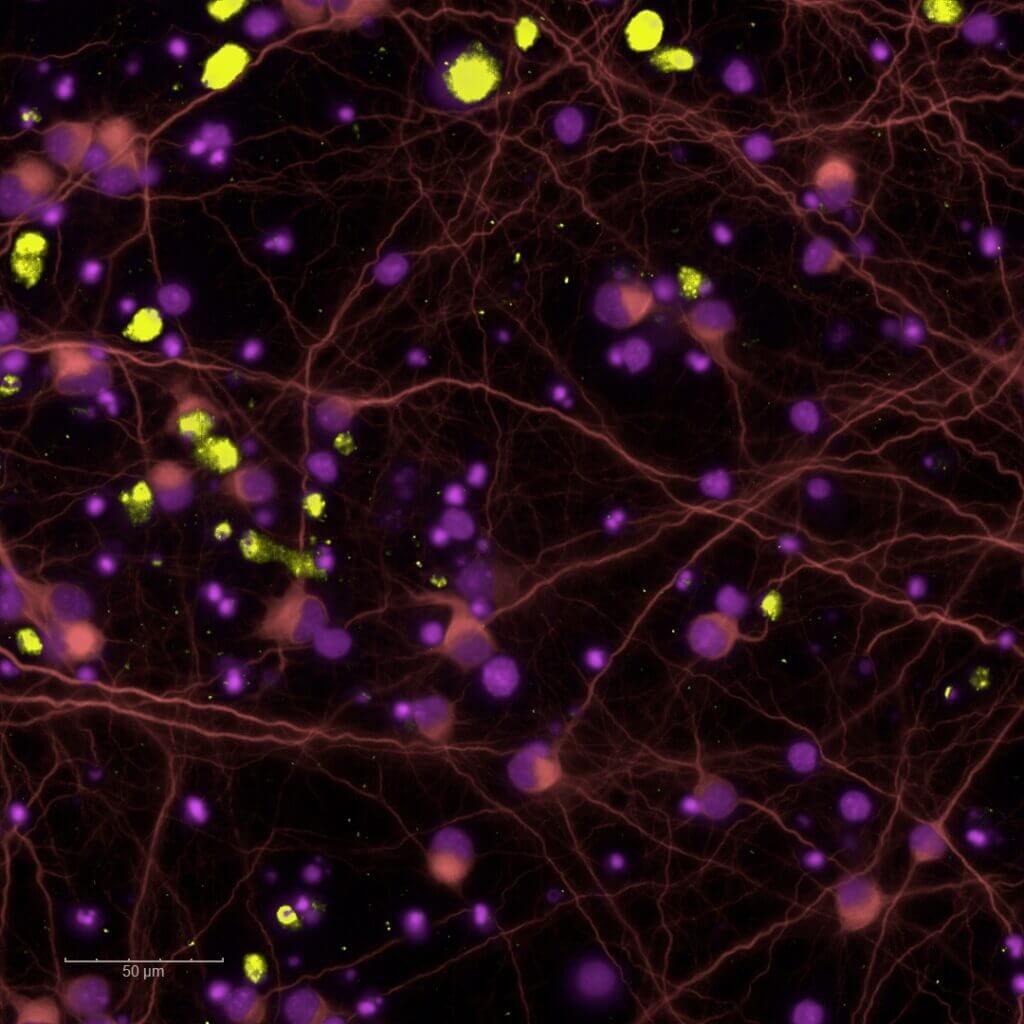
Modèles de pharmacologie in vitro en Neurologie & CNS
Accélérez le développement de vos thérapies pour le Système Nerveux Central (CNS) grâce à nos modèles de pharmacologie in vitro. De l’identification de leads à leur validation dans des systèmes cellulaires complexes, nos plateformes vous guident pour :
-> Criblez et identifier vos composés candidats neuroprotecteurs, anti-agrégants, thrombolytiques,
-> Analysez leurs mécanismes d’action sur des cibles spécifiques (protéinopathies, neurones, cellules gliales),
-> Améliorez la transposabilité vers la clinique grâce à l’utilisation de cerveau-sur-puce (NAMs).
Test d’agrégation et neutralisation
L’utilisation de nos oligomères humains offre la possibilité de tester l’efficacité de vos candidats à moduler leur cinétique d’agrégation ou à interférer spécifiquement avec ces sous- espèces protéiques, afin d’identifier les leads présentant le plus fort potentiel translationnel. Notre plateforme fournit une évaluation directe de vos candidats sur ces cibles pathologiques clés des protéinopathies.
Tests d’agrégation
Les protéinopathies se caractérisent par l’accumulation anormale de protéines mal conformées, qui s’assemblent en oligomères neurotoxiques. Evaluez le potentiel anti-agrégant de vos candidats dans un essai acellulaire (cell-free assay) ciblant ces espèces oligomériques. Ce protocole, basé sur une détection par fluorescence (ANS et Thioflavine T), suit la cinétique d’agrégation et la formation des espèces oligomériques pathologiques par spectrofluorimétrie.
Nos oligomères disponibles pour ces essais : amyloïde-β(1-42), Tau, α-synucléine.
Agrégation de l’amyloïde-β(1-42) humain
Ciblez l’agrégation de l’amyloïde-β1-42, acteur de la maladie d’Alzheimer, en utilisant nos oligomères produits à partir du peptide amyloïde-β synthétique non recombinant et sans endotoxine.
Agrégation de Tau humain
Ciblez l’agrégation de la protéine Tau, acteur des Tauopathies, en utilisant nos oligomères produits à partir de la protéine Tau humaine recombinante (isoforme 2N4R) avec un niveau d’endotoxines contrôlé (<1 EU/mL).
Agrégation de l’α-synucléine humain
Ciblez l’agrégation de l’α-synucléine humaine, protéine centrale de la maladie de Parkinson et des maladies à corps de Lewy, en utilisant nos oligomères produits à partir de la protéine α-synucléine humaine recombinante avec un niveau d’endotoxines contrôlé (<1 EU/mL).
Détection et reconnaissance des oligomères
Les protéinopathies se caractérisent par l’accumulation anormale de protéines mal conformées, qui s’assemblent en oligomères neurotoxiques. Evaluez le potentiel de neutralisation de vos candidats dans un essai acellulaire (cell-free assay) ciblant ces espèces oligomériques. Ce protocole, basé sur des immunoessais (Dot-blot), caractérise la reconnaissance des agrégats par vos candidats et fournissent une vue complète de leur efficacité et de leur mécanisme d’action.
Nos oligomères disponibles pour ces essais : amyloïde-β(1-42), Tau, α-synucléine.
Amyloïde-β(1-42) humain
Ciblez la neutralisation de l’amyloïde-β1-42, acteur de la maladie d’Alzheimer, en utilisant nos oligomères produits à partir du peptide amyloïde-β synthétique non recombinant et sans endotoxine.
Tau humain
Ciblez la neutralisation de la protéine Tau, acteur des Tauopathies, en utilisant nos oligomères produits à partir de la protéine Tau humaine recombinante (isoforme 2N4R) avec un niveau d’endotoxines contrôlé (<1 EU/mL).
α-synucléine humain
Ciblez la neutralisation de l’α-synucléine, protéine centrale de la maladie de Parkinson et des maladies à corps de Lewy, en utilisant nos oligomères produits à partir de la protéine α-synucléine humaine recombinante avec un niveau d’endotoxines contrôlé (<1 EU/mL).
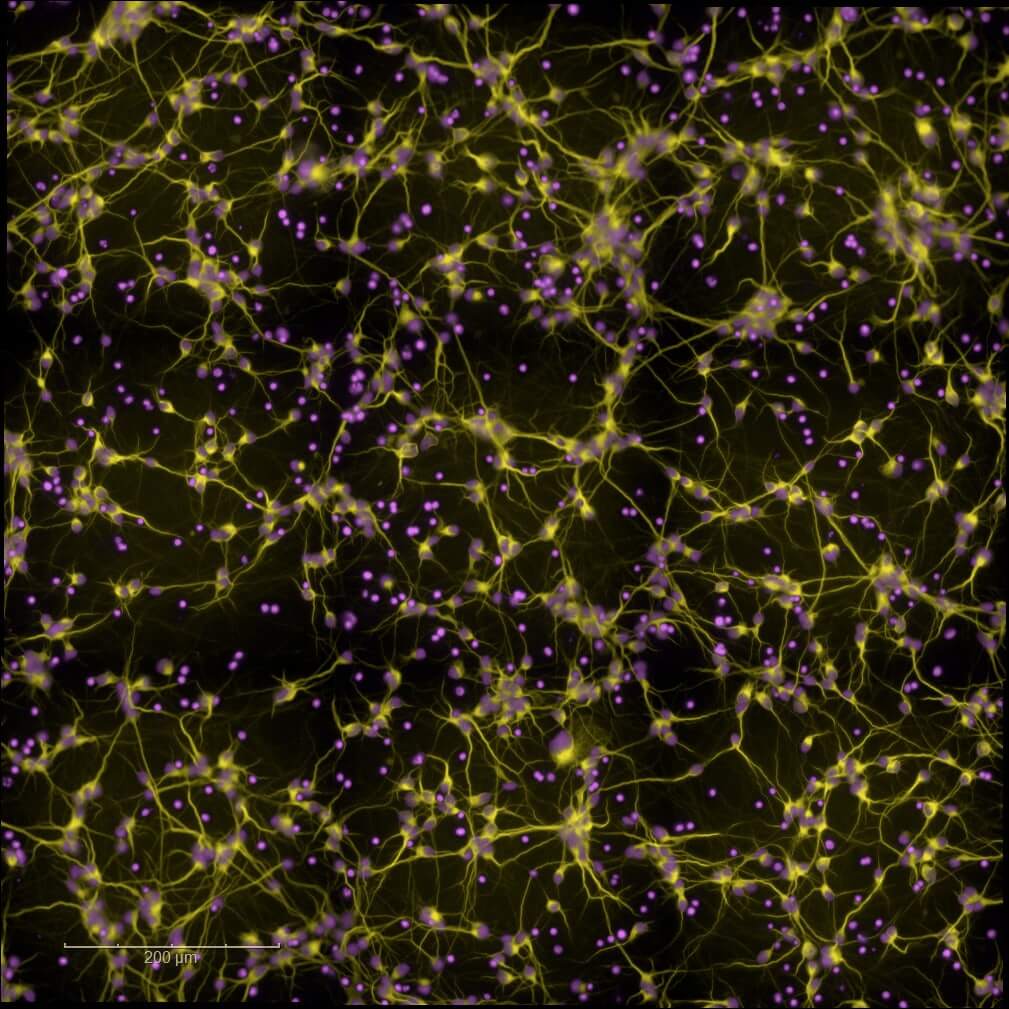
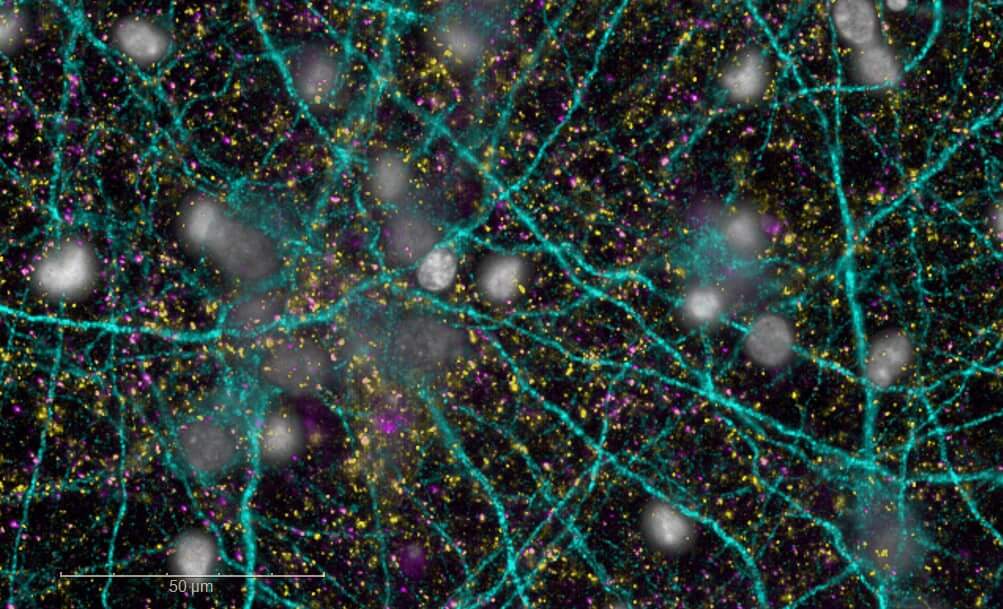
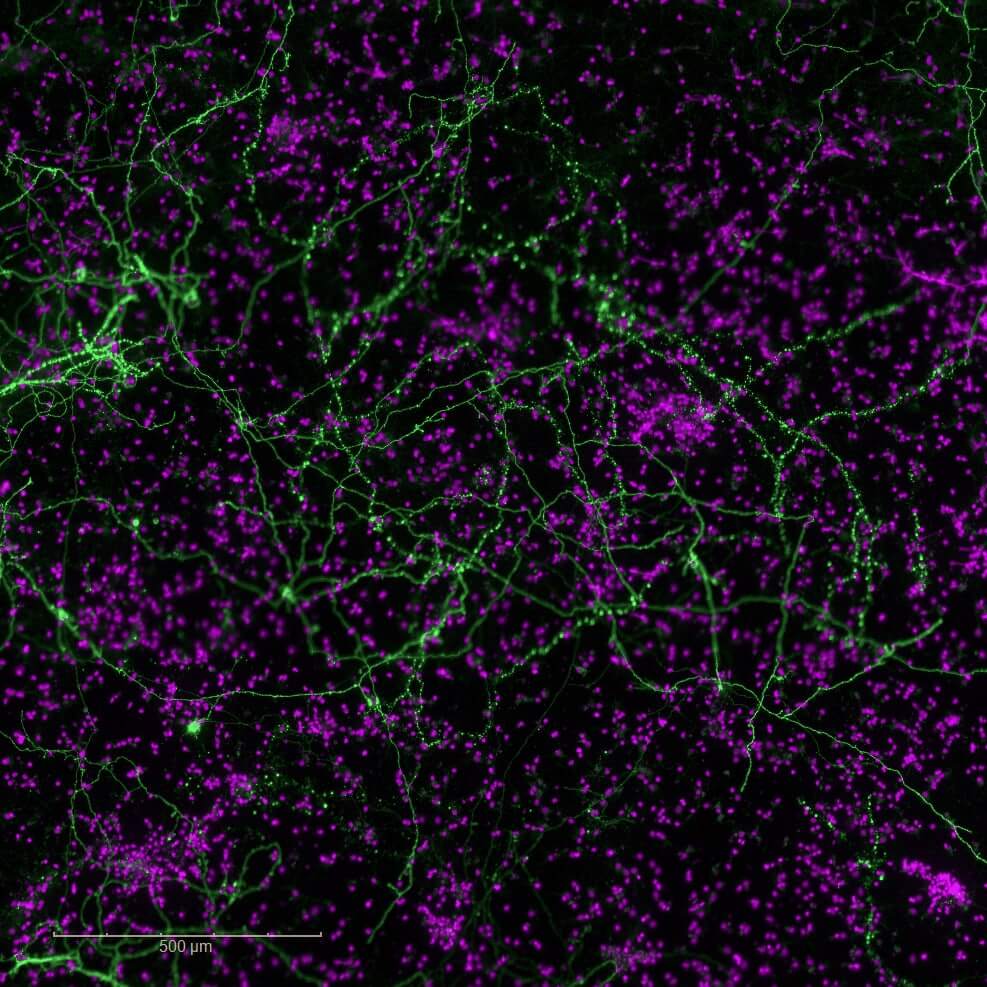
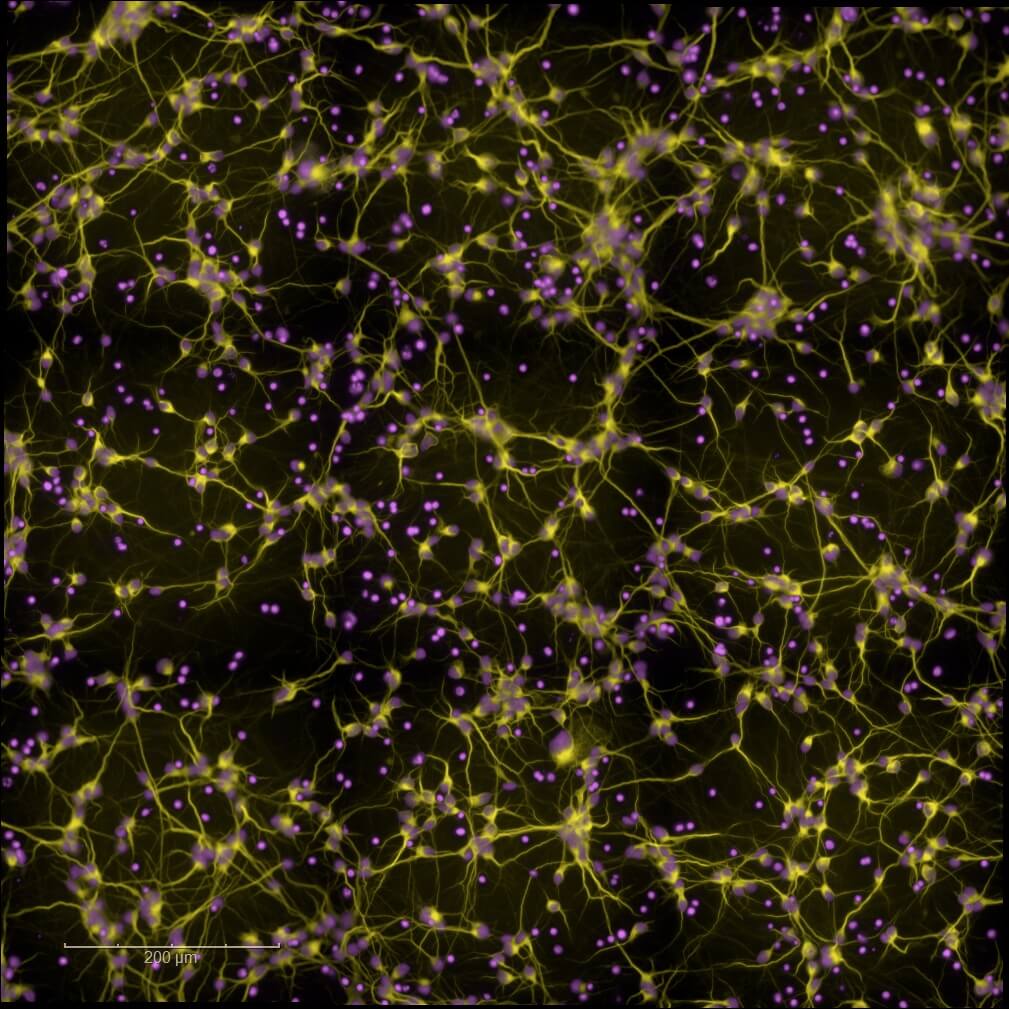
Cellules primaires et humaines (hiPSCs)
Validez et optimisez vos leads grâce à nos plateformes de criblage à haut contenu (High Content Imaging). Utilisez nos modèles de cellules primaires de rongeur ou de cellules humaines neuronales, gliales (hiPSCs, cellules souches pluripotentes induites) et nos analyses multi-paramètres pour une sélection de vos candidats et une progression éclairée vers le développement préclinique avancé.
Maladie d'Alzheimer
Cytotoxicité induite par les oligomères amyloïde-β(1-42) humains
L’efficacité de vos candidats est évaluée rapidement grâce à ce modèle cellulaire de maladie d’Alzheimer. Ce criblage primaire repose sur l’exposition de neurones primaires corticaux de rongeurs aux oligomères solubles amyloïde-β(1-42) humains. La viabilité neuronale est quantifiée par un test d’activité métabolique fournissant les données nécessaires pour identifier, optimiser et prioriser vos candidats les plus prometteurs en vue d’études mécanistiques avancées.
Cytotoxicité induite par les oligomères Tau humains
L’efficacité de vos candidats est évaluée rapidement grâce à ce modèle cellulaire de tauopathies. Ce criblage primaire repose sur l’exposition de neurones primaires corticaux de rongeurs aux oligomères solubles Tau humains. La viabilité neuronale est quantifiée par un test d’activité métabolique fournissant les données nécessaires pour identifier, optimiser et prioriser vos candidats les plus prometteurs en vue d’études mécanistiques avancées.
Neurodégénérescence induite par les oligomères amyloïde-β(1-42) humains
Au-delà de la viabilité, ce modèle, utilisant des neurones primaires corticaux de rongeurs, reproduit la cascade neurotoxique de la maladie d’Alzheimer, induite par les oligomères solubles amyloïde-β(1-42) humains, et quantifie la dégénérescence synaptique précoce, la perte progressive des neurites et la mort neuronale finale. L’analyse multi-paramètres fournit les données nécessaires pour révéler le mécanisme d’action et le potentiel modificateur de maladie de vos candidats.
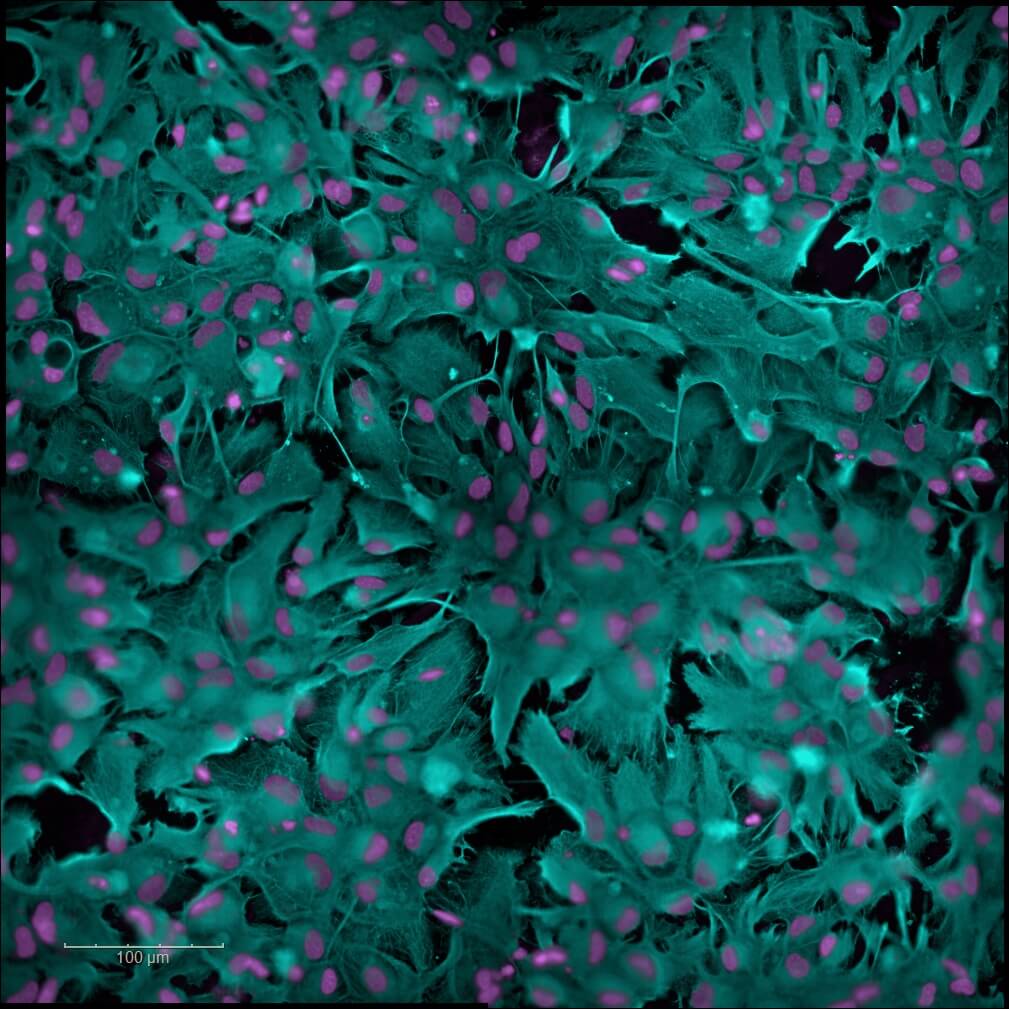
Neuroinflammation
La neuroinflammation est un mécanisme pathologique commun à plusieurs maladies du neurologiques, dont la maladie d’Alzheimer. Notre modèle d’astrocytes dérivés d’iPSC humaines permet d’évaluer les propriétés anti-inflammatoires de vos candidats. L’état neuroinflammatoire pathologique est induit en utilisant un cocktail de cytokines pro-inflammatoires (TNFα, IL-1β) ou en exposant les cellules à des oligomères pathologiques. L’analyse multi-paramètres mesure la modulation de l’astrogliose et identifie les candidats capables de rétablir un environnement glial physiologique ; une stratégie prometteuse pour le développement de thérapies dans les maladies neurodégénératives et les pathologies du CNS.
Toxicité induite par le glutamate : culture 2D
Notre modèle 2D permet un criblage rapide et fiable de composés ciblant l’excitotoxicité sur neurones primaires corticaux de rongeurs exposés à un excès de glutamate, avec MK801 comme traitement de référence.
Notre plateforme d’imagerie à haut contenu assure un criblage à moyen débit des effets du glutamate à des concentrations non cytotoxiques induisant une diminution de la densité synaptique ou une altération du réseau neuritique.
L’excitotoxicité est un mécanisme physiopathologique impliqué dans de nombreuses maladies neurologiques, y compris les maladies neurodégénératives.
Toxicité induite par le glutamate : organe-sur-puce
L’excitotoxicité est un mécanisme physiopathologique impliqué dans de nombreuses maladies neurologiques, y compris les maladies neurodégénératives.
Notre modèle de cerveau-sur-puce est conçu pour mimer l’excitotoxicité en appliquant du glutamate spécifiquement dans une chambre synaptique située à l’interface entre deux populations de neurones distantes (i.e. cultivées dans des environnements microphysiologiques indépendants). Notre plateforme de microfluidique couplée à l’imagerie à haut contenu assure un criblage à moyen débit des effets de votre composé sur la synapse isolée, à distance du soma, et exposée à un excès de glutamate.
Recapture du glutamate par les astrocytes
Les astrocytes jouent un rôle clé dans l’homéostasie de la synapse et la prévention de l’excitotoxicité en capturant l’excès de glutamate extracellulaire. Ce mécanisme est altéré chez les astrocytes réactifs dans les maladies neuroinflammatoires, et notamment les maladies neurodégénératives.
Notre modèle d’astrogliose permet de cribler vos molécules ciblant la recapture du glutamate dans une culture d’astrocytes dérivés d’iPSC humaines activés par un cocktail de cytokines. L’activation de la voie NFκB est également un read-out proposé en routine grâce à notre plateforme d’imagerie à haut contenu.
Maladie de Parkinson
Cytotoxicité induite par les oligomères α-synucléine humains
L’efficacité de vos candidats est évaluée rapidement grâce à ce modèle cellulaire de synucléinopathie. Ce criblage primaire repose sur l’exposition de neurones primaires corticaux de rongeurs aux oligomères solubles α-synucléine humains. La viabilité neuronale est quantifiée par un test d’activité métabolique fournissant les données nécessaires pour identifier, optimiser et prioriser vos candidats les plus prometteurs en vue d’études mécanistiques avancées.
Neurodégénérescence dopaminergique induite par les oligomères α-synucléine humains
Notre modèle, utilisant des neurones mésencéphaliques primaires de rongeur enrichis en neurones dopaminergiques, exposés à des oligomères α-synucléine humains, évalue spécifiquement la dégénérescence progressive de cette population neuronale clé. L’analyse multi-paramètres fournit les données nécessaires pour révéler le potentiel modificateur des synucléinopathies de vos candidats.
Neurodégénérescence dopaminergique induite par 6-OHDA
Notre modèle, utilisant des neurones mésencéphaliques primaires de rongeur exposés au 6-hydroxydopamine (6-OHDA), cible spécifiquement les neurones dopaminergiques et mime un stress oxydatif toxique. Ce test permet d’évaluer les propriétés neuroprotectrices de vos candidats pour contrecarrer ce mécanisme clé de la maladie de Parkinson.
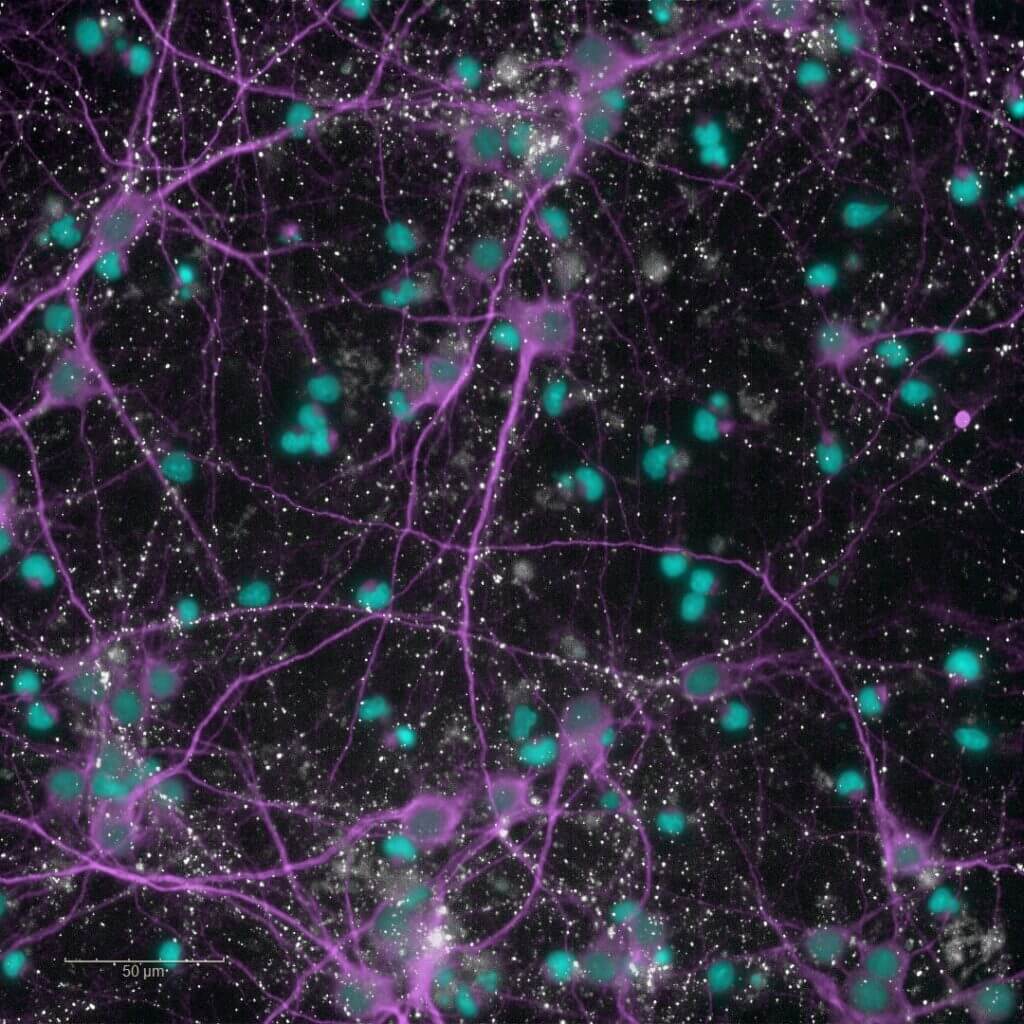
Modèles de neuroplasticité
Synaptogenèse et neuritogenèse
Notre modèle évalue directement la synaptogenèse (formation de nouvelles synapses) et la neuritogenèse (croissance et arborisation neuritique) sur des neurones primaires corticaux de rongeurs. En ciblant ces mécanismes fondamentaux de la plasticité, identifiez des candidats prometteurs pour favoriser la régénération des circuits neuronaux et contrecarrer la déconnexion synaptique et la perte neuronale caractéristiques des troubles neurodégénératifs.
Plasticité synaptique ciblée en Cerveau-sur-puce
Notre modèle de cerveau-sur-puce cible spécifiquement le compartiment synaptique pour quantifier directement la synaptogenèse (formation de nouvelles synapses) et la neuritogenèse (croissance et arborisation neuritique) sur des neurones primaires corticaux de rongeurs. En se focalisant sur ces mécanismes fondamentaux de la plasticité, identifiez des candidats prometteurs pour favoriser la régénération des circuits neuronaux et contrecarrer la déconnexion synaptique et la perte neuronale caractéristiques des troubles neurodégénératifs.
Modèles de neuroinflammation
Maladie d’Alzheimer
La neuroinflammation est un mécanisme pathologique commun à plusieurs maladies du neurologiques, dont la maladie d’Alzheimer. Notre modèle d’astrocytes dérivés d’iPSC humaines permet d’évaluer les propriétés anti-inflammatoires de vos candidats. L’état neuroinflammatoire pathologique est induit en exposant les cellules à des oligomères pathologiques. L’analyse multi-paramètres mesure la modulation de l’astrogliose et identifie les candidats capables de rétablir un environnement glial physiologique ; une stratégie prometteuse pour le développement de thérapies dans les maladies neurodégénératives et les pathologies du CNS.
Cytokines
La neuroinflammation est un mécanisme pathologique commun à plusieurs maladies du neurologiques, dont la maladie d’Alzheimer. Notre modèle d’astrocytes dérivés d’iPSC humaines permet d’évaluer les propriétés anti-inflammatoires de vos candidats. L’état neuroinflammatoire pathologique est induit en utilisant un cocktail de cytokines pro-inflammatoires (TNFα, IL-1β). L’analyse multi-paramètres mesure la modulation de l’astrogliose et identifie les candidats capables de rétablir un environnement glial physiologique ; une stratégie prometteuse pour le développement de thérapies dans les maladies neurodégénératives et les pathologies du CNS.
Accident Vasculaire Cérébral (AVC)
Retrouvez nos modèles d’AVC in vitro pour tester vos candidats médicaments sur sang humain. Toutes les informations dans notre page dédiée à nos services précliniques en maladies neurovasculaires.
Toxicité induite par le glutamate : culture 2D
Notre modèle 2D permet un criblage rapide et fiable de composés ciblant l’excitotoxicité sur cultures primaires de neurones de rongeur exposés à un excès de glutamate, avec le MK801 comme traitement de référence.
Notre plateforme d’imagerie à haut contenu assure un criblage à moyen débit des effets du glutamate, à des concentrations mimant l’excitotoxicité aigüe, mais également à des concentrations non cytotoxiques induisant une diminution de la densité synaptique ou une altération du réseau neuritique.
L’excitotoxicité est un mécanisme physiopathologique clé de la cascade ischémique consécutive à un AVC. Elle intervient dès la phase aigüe de l’ischémie (quelques minutes à quelques heures) et perdure au cours des phases post-ischémiques (inflammation, remodelage synaptique, hyperexcitabilité épileptogène…).
Toxicité induite par le glutamate : organe-sur-puce
L’excitotoxicité est un mécanisme physiopathologique clé de l’AVC ischémique qui joue en autre un rôle significatif dans la consolidation de la lésion cérébrale à distance du cœur ischémique.
Notre modèle de cerveau-sur-puce est conçu pour mimer l’excitotoxicité secondaire en appliquant du glutamate spécifiquement dans une chambre synaptique située à l’interface entre deux populations de neurones distantes (i.e. cultivées dans des environnements microphysiologiques indépendants).
Notre plateforme de microfluidique couplée à l’imagerie à haut contenu assure un criblage à moyen débit des effets de votre composé sur la synapse isolée, à distance du soma, et exposée à un excès de glutamate.
Recapture du glutamate par les astrocytes
Les astrocytes jouent un rôle clé dans l’homéostasie de la synapse et la prévention de l’excitotoxicité en capturant l’excès de glutamate extracellulaire. Ce mécanisme est altéré chez les astrocytes réactifs au cours de la phase inflammatoire post-ischémique.
Notre modèle d’astrogliose permet de cribler vos molécules ciblant la recapture du glutamate dans une culture d’astrocytes humains (iPSC) activés par un cocktail de cytokines. L’activation de la voie NFκB est également un read-out proposé en routine grâce à notre plateforme d’imagerie à haut contenu.
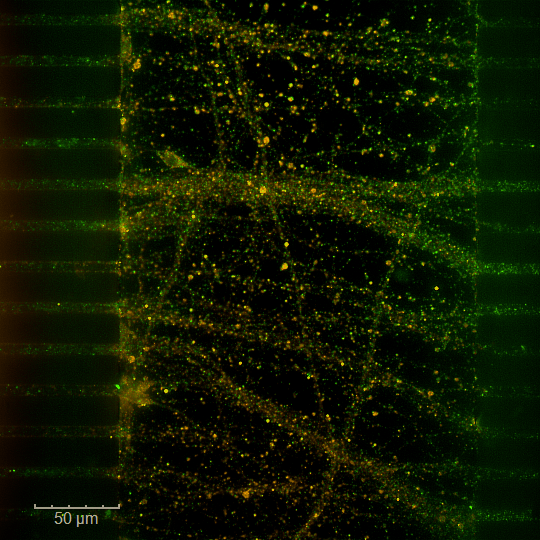
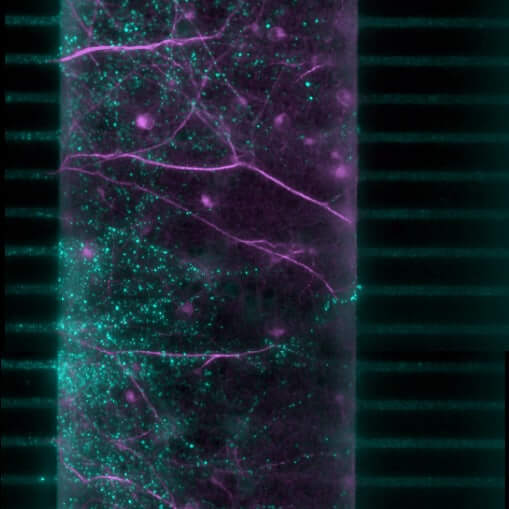
Cerveau-sur-puce – NAMs
Découvrez les nouvelles approches méthodologiques (NAMs) pour des recherches optimisées dans un système complexe et intégré grâce à notre technologie cerveau-sur-puce (BoC). Notre plateforme BoC reproduit l’architecture neuronale et les interactions cellulaires grâce à un système microfluidique compartimenté. C’est l’outil ultime pour confirmer le potentiel de vos candidats, en ciblant spécifiquement des mécanismes, pour une évaluation prédictive de leur efficacité contre la neurodégénérescence et la propagation des protéinopathies.
Passez à un niveau supérieur de modélisation pour vos projets les plus exigeants.
Modèles de neuroplasticité
Plasticité synaptique ciblée en Cerveau-sur-puce
Notre modèle de cerveau-sur-puce cible spécifiquement le compartiment synaptique pour quantifier directement la synaptogenèse (formation de nouvelles synapses) et la neuritogenèse (croissance et arborisation neuritique) sur des neurones primaires corticaux de rongeurs. En se focalisant sur ces mécanismes fondamentaux de la plasticité, identifiez des candidats prometteurs pour favoriser la régénération des circuits neuronaux et contrecarrer la déconnexion synaptique et la perte neuronale caractéristiques des troubles neurodégénératifs.
Excitotoxicité
Toxicité induite par le glutamate : organe-sur-puce
L’excitotoxicité est un mécanisme physiopathologique impliqué dans de nombreuses maladies neurologiques, y compris les maladies neurodégénératives.
Notre modèle de cerveau-sur-puce est conçu pour mimer l’excitotoxicité en appliquant du glutamate spécifiquement dans une chambre synaptique située à l’interface entre deux populations de neurones distantes (i.e. cultivées dans des environnements microphysiologiques indépendants). Notre plateforme de microfluidique couplée à l’imagerie à haut contenu assure un criblage à moyen débit des effets de votre composé sur la synapse isolée, à distance du soma, et exposée à un excès de glutamate.
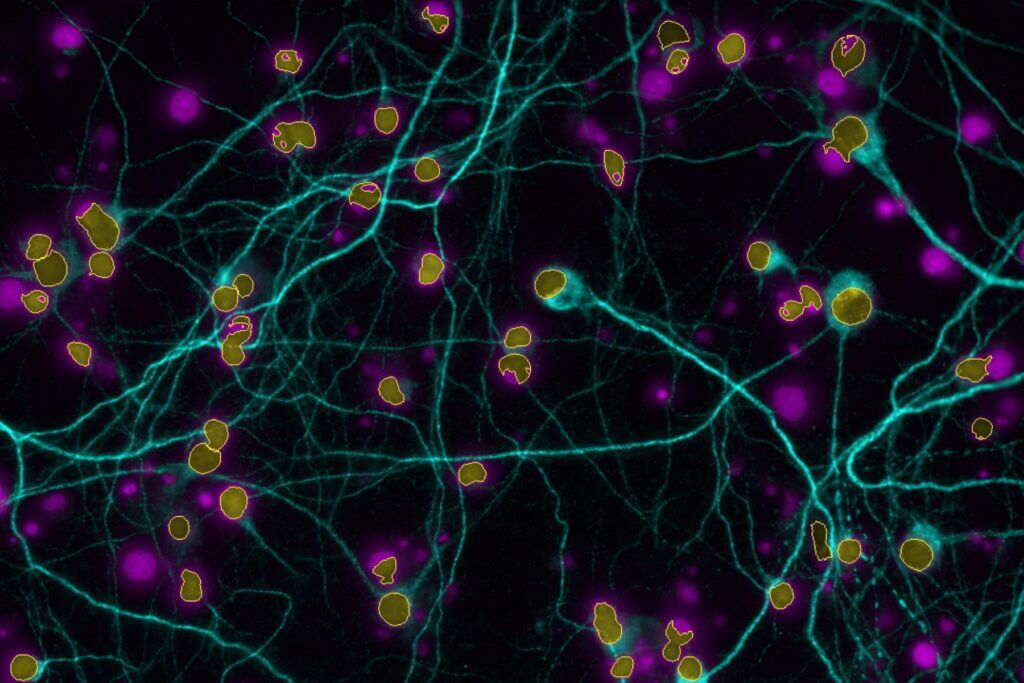
High-Content Imaging
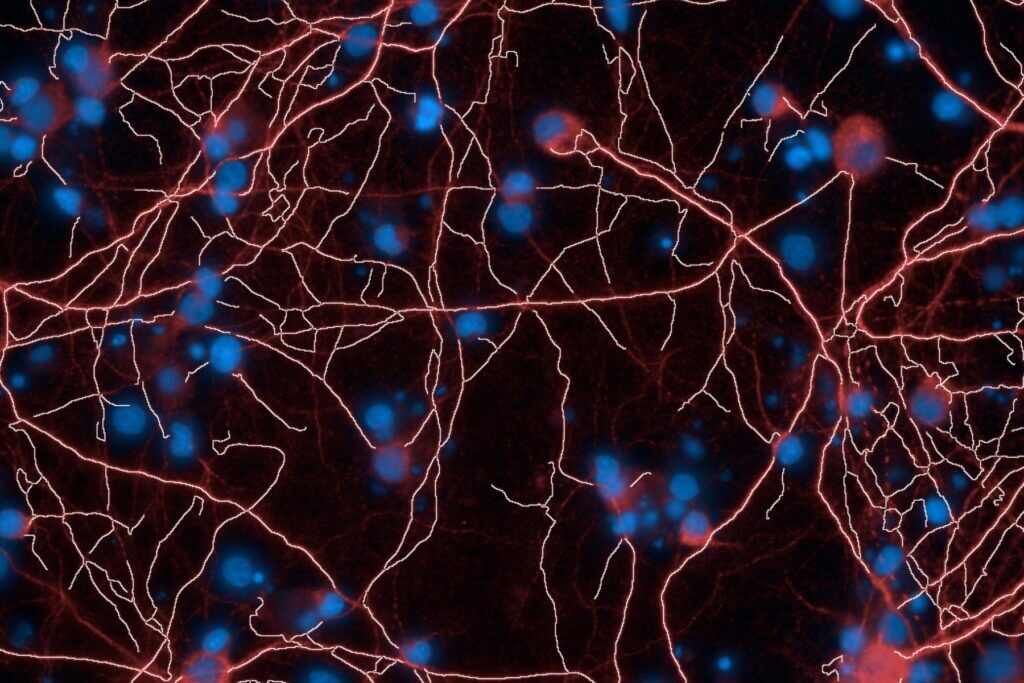
Microfluidique et cerveaux-sur-puce

Animaleries petits et gros animaux
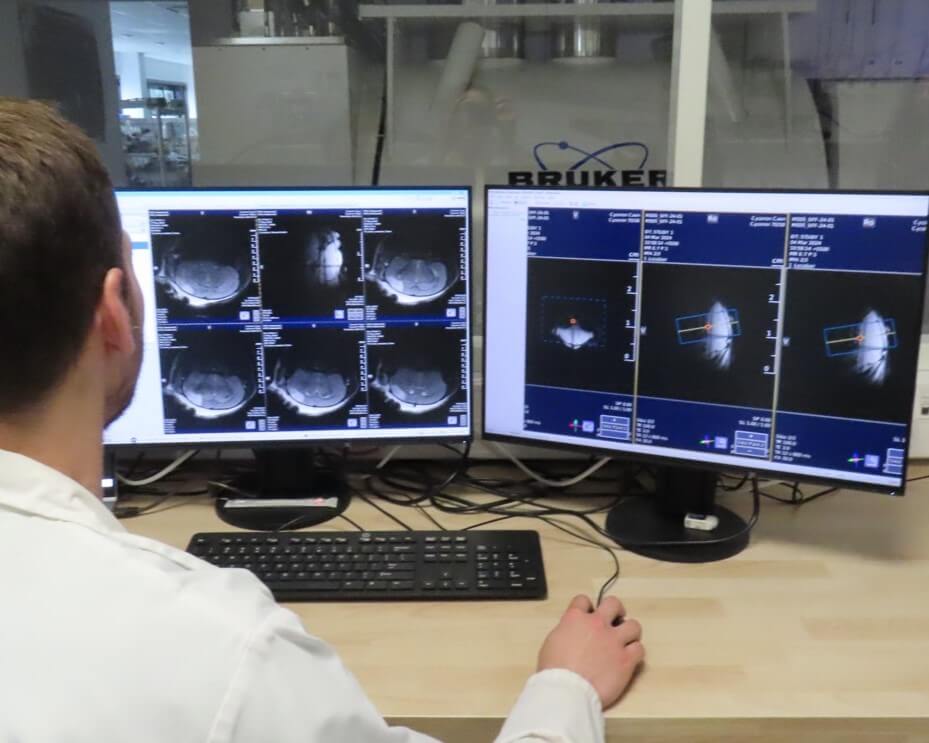
Imagerie médicale préclinique

Immunohistochimie, immunofluorescence et histologie
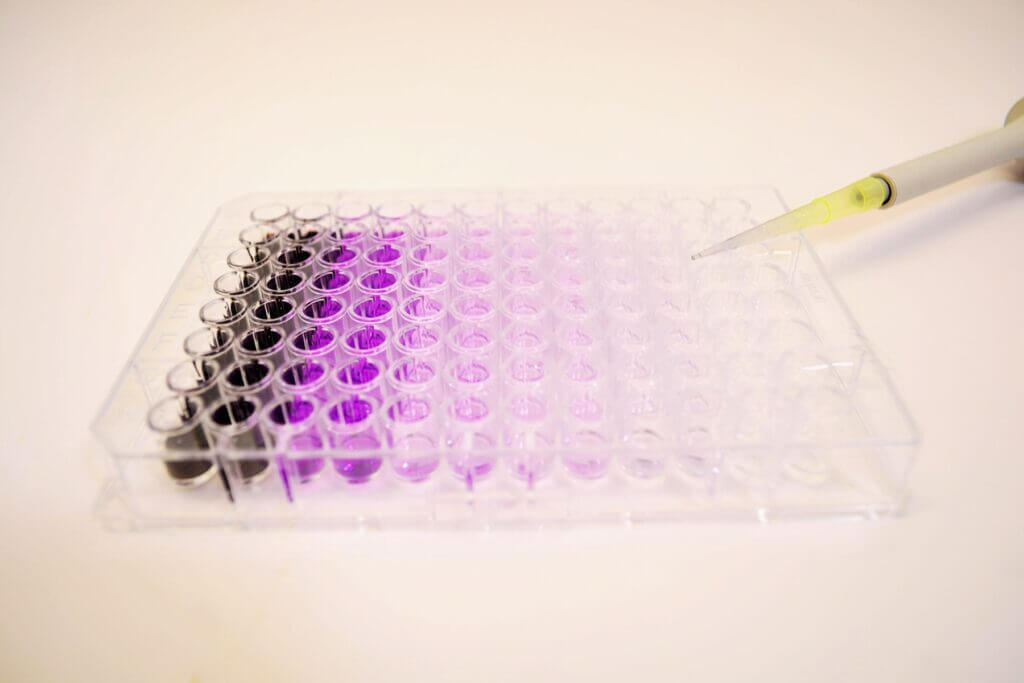
Immunodosage
Les effets de vos molécules peuvent être évalués grâce à des approches complémentaires et multi-échelles.